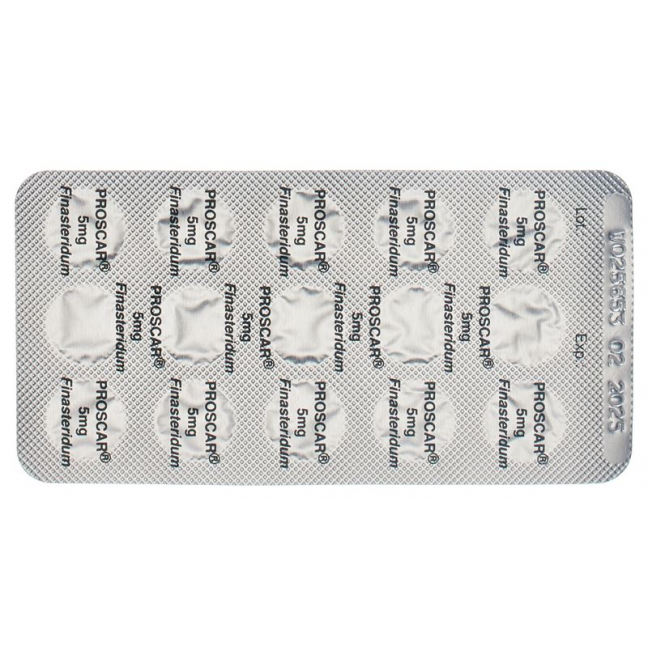
Проскар плівкові таблетки 5 мг 28 шт
Proscar 5 mg 30 Filmtabletten
-
10553.53 RUB
Дата доставки:
24.12.2025 - 07.01.2026
При оплате криптовалютой:
Ваша прибыль 1055.35 RUB / 12.35 USDT
- Наявність: В наявності
- Виробник: Organon GmbH
- Модель: 7750534
- ATC-код G04CB01
- EAN 7680517740014
Опис
Was ist Proscar und wann wird es angewendet?
Proscar ist ein Arzneimittel zur Behandlung der gutartigen Prostatavergrösserung (Benigne Prostatahyperplasie / Prostata = Vorsteherdrüse des Mannes).
Proscar darf nur auf Verschreibung des Arztes oder der Ärztin eingenommen werden.
Was sollte dazu beachtet werden?
Gutartige Prostatavergrösserung ist eine verbreitete, mit zunehmendem Alter häufiger werdende Krankheit, die sich über viele Jahre langsam entwickelt. Bei fortgeschrittener Vergrösserung der Prostata können Beschwerden beim Wasserlösen und im Bereich der Blase auftreten. Typisch dafür sind: Verzögerung zu Beginn der Blasenentleerung, Nachtröpfeln nach dem Wasserlösen, verminderte Stärke des Harnstrahls, ein- bis mehrfache Unterbrechungen im Harnfluss während des Wasserlösens, Gefühl der unvollständig entleerten Blase, Schmerzen und Brennen während des Wasserlösens, notwendiges Pressen zur Ingangsetzung des Harnflusses, nasse Kleider, dringendes Bedürfnis Wasser zu lösen, häufiges Wasserlösen bei Tag und bei Nacht. Bekannte Komplikationen einer unbehandelten gutartigen Prostatavergrösserung sind: wiederholt auftretende Harnwegsinfektionen, Nierenversagen, akute Harnverhaltung und dadurch bedingte chirurgische Eingriffe.
Proscar beeinflusst die Ursache des krankhaften Prostatawachstums. Es vermag die vergrösserte Prostata zu verkleinern und damit die oben erwähnten Beschwerden zu verbessern. Eine gutartige Prostatavergrösserung entwickelt sich über eine längere Zeit, deshalb erfordert die Rückbildung der vergrösserten Prostata in der Regel eine lange Therapie mit Proscar, obwohl in manchen Fällen eine rasche Besserung der Symptome beobachtet werden konnte.
Unabhängig davon, ob Sie eine Verbesserung oder Änderung Ihrer Symptome beobachten, kann die Therapie mit Proscar das Risiko für eine plötzliche Harnverhaltung oder für einen operativen Eingriff senken.
Befolgen Sie die Anweisungen Ihres Arztes bzw. Ihrer Ärztin. Beim Absetzen von Proscar kann sich die Prostata wieder vergrössern und die Symptome der benignen Prostatahyperplasie können wieder auftreten. Suchen Sie Ihren Arzt bzw. Ihre Ärztin für regelmässige Kontrolluntersuchungen auf. Proscar kann die Resultate einer Blutuntersuchung, den sogenannten PSA-Test beeinflussen. Wenn bei Ihnen ein PSA-Test durchgeführt wird, weisen Sie Ihren Arzt bzw. Ihre Ärztin darauf hin, dass Sie Proscar einnehmen.
Wann darf Proscar nicht angewendet werden?
Nehmen Sie Proscar nicht ein, wenn Sie auf irgendeinen der Inhaltsstoffe überempfindlich (allergisch) reagieren.
Proscar darf nicht von Frauen und Kindern eingenommen werden.
Wann ist bei der Einnahme von Proscar Vorsicht geboten?
Berichten Sie Ihrem Arzt bzw. Ihrer Ärztin über alle medizinischen Probleme, die Sie haben oder früher gehabt haben, sowie über Ihnen bekannte Allergien.
Wenn Sie Veränderungen in Ihrem Brustgewebe feststellen, wie z.B. Knoten, Schmerzen, Vergrösserung der Brust oder Ausfluss aus den Brustwarzen, sollten Sie sich umgehend an Ihren Arzt bzw. Ihre Ärztin wenden. Diese Anzeichen weisen möglicherweise auf eine ernsthafte Erkrankung wie Brustkrebs hin.
Über männliche Infertilität und/oder schlechte Samenqualität wurde bei einigen Männern unter Einnahme von Proscar berichtet. Über eine Verbesserung der Samenqualität nach Absetzen des Arzneimittels wurde berichtet.
Frauen im gebährfähigen Alter sollten den Kontakt mit Proscar durch Anfassen von zerbrochenen Filmtabletten vermeiden, da wegen der möglichen Aufnahme des Wirkstoffs während einer Schwangerschaft die normale Entwicklung der äusseren Geschlechtsorgane eines männlichen Kindes beeinträchtigt werden kann. Proscar Filmtabletten sind beschichtet, bei normaler Handhabung ist kein Kontakt mit dem Wirkstoff möglich, ausser die Filmtabletten sind zerdrückt oder zerbrochen.
Proscar geht normalerweise keine Wechselwirkungen mit anderen Arzneimitteln ein. Informieren Sie jedoch Ihren Arzt bzw. Ihre Ärztin immer über alle Arzneimittel, die Sie gerade einnehmen oder einzunehmen gedenken, auch über solche, die Sie ohne Rezept erhalten.
Informieren Sie Ihren Arzt oder Apotheker bzw. Ihre Ärztin oder Apothekerin, wenn Sie an anderen Krankheiten leiden, Allergien haben oder andere Arzneimittel (auch selbstgekaufte!) einnehmen oder äusserlich anwenden!
Darf Proscar während einer Schwangerschaft oder in der Stillzeit eingenommen werden?
Proscar darf nicht von Frauen eingenommen werden.
Wie verwenden Sie Proscar?
Die übliche Dosierung beträgt eine Filmtablette Proscar täglich, unabhängig von den Mahlzeiten.
Nehmen Sie Proscar einmal täglich wie vorgeschrieben ein. Sollten Sie trotzdem einmal eine Dosis vergessen, so nehmen Sie keine Extradosis ein. Nehmen Sie einfach Ihren üblichen Einnahmeplan von einer Filmtablette pro Tag wieder auf.
Sollten Sie zu viele Filmtabletten aufs Mal eingenommen haben, so setzen Sie sich sofort mit Ihrem Arzt bzw. Ihrer Ärztin in Verbindung.
Ändern Sie nicht von sich aus die verschriebene Dosierung des Arzneimittels. Wenn Sie glauben, das Arzneimittel wirke zu schwach oder zu stark, so sprechen Sie mit Ihrem Arzt oder Apotheker bzw. Ihrer Ärztin oder Apothekerin (siehe auch Kapitel «Was ist ferner zu beachten?»).
Welche Nebenwirkungen kann Proscar haben?
Folgende Nebenwirkungen können bei der Einnahme von Proscar auftreten:
Häufig beobachtete unerwünschte Wirkungen, deren Ursache als möglicherweise, wahrscheinlich oder sicher mit dem Präparat in Verbindung gebracht wurde, waren: Impotenz, abnehmende Libido (Geschlechtstrieb) und vermindertes Ejakulat-Volumen.
Im Laufe der Einnahme von Proscar verschwanden diese unerwünschten Wirkungen in einigen Fällen. Wenn die Symptome andauerten, waren sie beim Absetzen gewöhnlich reversibel.
Gelegentlich wurde über unerwünschte Wirkungen einschliesslich Ejakulationsstörungen, Druckempfindlichkeit der Brust und/oder Vergrösserung der Brust sowie Hautausschlag berichtet.
Selten wurde über unerwünschte Wirkungen einschliesslich Hodenschmerzen oder allergische Reaktionen wie Juckreiz, Nesselsucht, Schwellung der Lippen, der Zunge, des Rachens und des Gesichts berichtet.
Wenn Sie Veränderungen in Ihrem Brustgewebe feststellen, wie z.B. Knoten, Schmerzen oder Ausfluss aus den Brustwarzen, sollten Sie sich umgehend an Ihren Arzt bzw. Ihre Ärztin wenden (siehe «Wann ist bei der Einnahme von Proscar Vorsicht geboten?»).
In sehr seltenen Fällen wurde über Brustkrebs bei Männern berichtet.
In Einzelfällen wurde
- über Blut im Sperma;
- über eine nach Absetzen des Arzneimittels fortbestehende Unfähigkeit zur Erektion;
- über nach Absetzen des Arzneimittels fortbestehende Ejakulationsprobleme;
- über eine nach Absetzen des Arzneimittels fortbestehende Libidoreduktion (Geschlechtstrieb);
- über Depression berichtet.
Auch wenn Sie Nebenwirkungen bemerken, die hier nicht beschrieben sind, sollten Sie Ihren Arzt oder Apotheker bzw. Ihre Ärztin oder Apothekerin informieren.
Was ist ferner zu beachten?
Lagerungshinweis
Für Kinder unerreichbar aufbewahren.
In der Originalverpackung vor Licht geschützt bei unter 30 °C aufbewahren.
Das Arzneimittel darf nur bis zu dem auf der Packung mit «EXP» bezeichneten Datum verwendet werden.
Weitere Hinweise
Weitere Auskünfte erteilt Ihnen Ihr Arzt oder Apotheker bzw. Ihre Ärztin oder Apothekerin. Diese Personen verfügen über die ausführliche Fachinformation.
Was ist in Proscar enthalten?
Wirkstoffe
Eine Filmtablette Proscar enthält als Wirkstoff 5 mg Finasterid.
Hilfsstoffe
Blauer Farbstoff: Indigotin (E 132) sowie weitere Hilfsstoffe.
Zulassungsnummer
51774 (Swissmedic).
Wo erhalten Sie Proscar? Welche Packungen sind erhältlich?
In Apotheken nur gegen ärztliche Verschreibung
Das Arzneimittel ist in Kalenderpackungen zu 28 und 30 oder 98 und 105 Filmtabletten erhältlich.
Zulassungsinhaberin
MSD MERCK SHARP & DOHME AG, Luzern.
Diese Packungsbeilage wurde im Dezember 2019 letztmals durch die Arzneimittelbehörde (Swissmedic) geprüft.
S-WPPI-MK0906-5T-072018/0906-CHE-2019-021059
Qu’est-ce que Proscar et quand doit-il être utilisé?
Proscar est un médicament destiné au traitement d'une forme bénigne d'accroissement de volume de la prostate (hyperplasie bénigne de la prostate: HBP).
Proscar ne doit être pris que sur prescription du médecin.
De quoi faut-il tenir compte en dehors du traitement?
L'accroissement bénin du volume de la prostate est une maladie très répandue dont la fréquence augmente avec l'âge et qui se développe lentement sur de nombreuses années. Lors de l'accroissement progressif du volume de la prostate peuvent survenir des troubles au moment où l'on urine, de même que des problèmes au niveau de la vessie. Sont typiques de cet état: hésitation ou attente au début d'uriner, égouttement après avoir uriné, diminution de la force du jet urinaire, interruptions uniques ou répétées du flux urinaire pendant que l'on urine, sensation de vidange incomplète de la vessie, douleur et brûlure lorsque l'on urine, besoin de pousser pour commencer à uriner, vêtements mouillés, besoin urgent d'uriner et besoin fréquent d'uriner, de jour et de nuit. Des infections répétées des voies urinaires, des défaillances rénales de même qu'une rétention urinaire aiguë et les interventions chirurgicales en résultant sont des complications connues d'un accroissement bénin du volume de la prostate non traité.
Proscar influence la cause de la croissance pathologique de la prostate. Il a la capacité de réduire le volume de la prostate agrandie et par conséquent d'améliorer les troubles mentionnés ci-dessus. L'hyperplasie bénigne de la prostate se développe sur plusieurs années, raison pour laquelle la diminution du volume de la prostate agrandie exige normalement une thérapie à long terme avec Proscar; néanmoins, dans certain cas, une rapide amélioration des symptômes a été observée.
Indépendamment du fait, que vous observiez une amélioration ou une modification des symptômes, la thérapie avec Proscar peut diminuer le risque de rétention urinaire soudaine ou d'une intervention chirurgicale.
Suivez les recommandations de votre médecin. Lors de l'interruption de la prise de Proscar, la prostate peut à nouveau s'agrandir et les symptômes de l'hyperplasie bénigne de la prostate peuvent à nouveau apparaître.
Visitez votre médecin pour des contrôles réguliers. Proscar peut influencer les résultats d'un examen sanguin, le test du PSA. Si un test du PSA est fait, informez votre médecin que vous prenez Proscar.
Quand Proscar ne doit-il pas être pris?
Proscar ne doit pas être utilisé en cas d'allergie à l'un des composants du médicament.
Proscar ne doit pas être utilisé ni par les femmes, ni par les enfants.
Quelles sont les précautions à observer lors de la prise de Proscar?
Informez votre médecin de tous vos problèmes médicaux actuels ou passés, ainsi que de vos allergies connues.
Si vous observez des modifications du tissu mammaire telles que par exemple nodules, douleurs, augmentation du volume du sein ou écoulement de liquide à partir du mamelon, vous devez immédiatement en informer votre médecin. Ces symptômes peuvent éventuellement indiquer la présence d'une maladie sérieuse comme un cancer du sein.
On a rapporté des cas d'infertilité masculine et/ou de mauvaise qualité du sperme chez des hommes traités par Proscar. Une amélioration de la qualité du sperme après l'arrêt du médicament a été rapportée.
Les femmes en âge de procréer devraient éviter tout contact avec Proscar par la manipulation de comprimés pelliculés brisés, en raison d'une possible absorption du principe actif pendant la grossesse et du risque potentiel de malformations des organes externes d'enfants du sexe masculin qui en résulte. Les comprimés de Proscar étant pelliculés, une manipulation normale rend le contact avec le principe actif impossible sauf si les comprimés pelliculés sont écrasés ou brisés.
Proscar ne présente d'habitude aucune interaction avec d'autres médicaments. Vous devez néanmoins toujours informer votre médecin de tous les médicaments que vous prenez ou envisagez de prendre, même ceux que vous avez obtenus sans ordonnance.
Veuillez informer votre médecin ou votre pharmacien si vous souffrez d'autres maladies, vous êtes allergique ou si vous prenez déjà d'autres médicaments en usage interne ou externe (même en automédication!).
Proscar peut-il être pris pendant la grossesse ou l’allaitement?
Proscar ne doit pas être pris par des femmes.
Comment utiliser Proscar?
Le dosage habituel de Proscar est d'un comprimé pelliculé par jour, indépendamment des repas.
Prenez Proscar une fois par jour, comme prescrit. Si vous avez oublié de prendre votre dose journalière, ne prenez pas de dose supplémentaire. Continuez simplement la posologie habituelle d'un comprimé pelliculé par jour.
Prévenez immédiatement votre médecin si vous avez avalé trop de comprimés pelliculés à la fois.
Ne changez pas de votre propre chef le dosage prescrit. Adressez-vous à votre médecin ou à votre pharmacien si vous estimez que l'efficacité du médicament est trop faible ou au contraire trop forte (voir aussi «À quoi faut-il encore faire attention?»).
Quels effets secondaires Proscar peut-il provoquer?
La prise de Proscar peut provoquer les effets secondaires suivants:
On a observé fréquemment des effets indésirables dont la cause était peut-être, probablement ou sûrement à mettre en relation avec le médicament; il s'agissait d'impuissance, d'une baisse de la libido (appétit sexuel) et d'une diminution du volume de l'éjaculat.
Ces effets indésirables ont disparu dans quelques cas durant la prise de Proscar. En cas de persistance des symptômes, ceux-ci étaient habituellement réversibles à l'arrêt du traitement.
Des cas occasionnels d'effets indésirables comprenant des troubles de l'éjaculation, une sensibilité à la pression du sein et/ou un agrandissement du sein ainsi qu'une éruption cutanée ont été rapportés. De rares cas d'effets indésirables comprenant des douleurs testiculaires ou des réactions allergiques telles que démangeaisons, urticaire, gonflement des lèvres, de la langue, de la gorge et du visage ont été rapportés.
Si vous remarquez chez vous des modifications de votre tissu mammaire telles que des nodules, des douleurs ou un écoulement de liquide à partir du mamelon, vous devriez immédiatement en informer votre médecin (voir «Quelles sont les précautions à observer lors de la prise de Proscar?»).
Très rarement, des cas de cancers du sein chez l'homme ont été rapportés.
Des cas individuels:
- de sang dans le sperme,
- de persistance d'une incapacité d'avoir une érection après l'arrêt de l'administration du médicament,
- de persistance de problèmes d'éjaculation après l'arrêt de l'administration du médicament,
- de baisse de la libido (appétit sexuel) persistant après l'arrêt de l'administration du médicament
- et de dépression ont été rapportés.
De même, si vous remarquez des effets secondaires non mentionnés dans cette notice d'emballage, veuillez en informer votre médecin ou votre pharmacien.
À quoi faut-il encore faire attention?
Remarques concernant le stockage
Tenir hors de la portée des enfants.
A conserver dans l'emballage d'origine, à l'abri de la lumière et à une température inférieure à 30 °C.
Le médicament ne doit pas être utilisé au-delà de la date figurant après la mention «EXP» sur l'emballage.
Remarques complémentaires
Pour de plus amples renseignements, consultez votre médecin ou votre pharmacien qui disposent d'une information détaillée destinée aux professionnels.
Que contient Proscar?
Principes actifs
Un comprimé pelliculé de Proscar contient 5 mg de la substance active finastéride.
Excipients
Colorant bleu: indigotine (E 132) et autres excipients.
Numéro d'autorisation
51774 (Swissmedic).
Où obtenez-vous Proscar? Quels sont les emballages à disposition sur le marché?
En pharmacie, seulement sur ordonnance médicale.
Le médicament est disponible en emballages calendrier de 28 et 30 ou de 98 et 105 comprimés pelliculés.
Titulaire de l’autorisation
MSD MERCK SHARP & DOHME AG, Lucerne.
Cette notice d'emballage a été vérifiée pour la dernière fois en décembre 2019 par l'autorité de contrôle des médicaments (Swissmedic).
S-WPPI-MK0906-5T- 072018/0906-CHE-2019-021059
Che cos’è Proscar e quando si usa?
Proscar è un medicamento per trattare l'iperplasia prostatica benigna, ossia l'ingrossamento della prostata.
Proscar deve essere preso solo su prescrizione medica.
Di che cosa occorre inoltre tener conto durante il trattamento?
L'iperplasia prostatica benigna è una malattia molto diffusa, la cui frequenza aumenta con l'età e che si sviluppa lentamente, nel corso di molti anni. Se la prostata è notevolmente ingrossata, si possono manifestare disturbi durante la minzione e nella regione della vescica. Segni tipici sono: inizio ritardato della minzione, gocciolamento dopo la minzione, riduzione della forza del mitto urinario, singole o ripetute interruzioni del flusso urinario durante la minzione, sensazione di vescica non completamente vuota, dolori e bruciori durante la minzione, necessità di pressare per iniziare la minzione, biancheria bagnata, urgente necessità di urinare, frequente necessità di urinare di giorno e di notte. Complicazioni note di un'iperplasia prostatica benigna non trattata possono essere: infezioni ricorrenti delle vie urinarie, insufficienza renale e ritenzione urinaria acuta (compresi i necessari interventi chirurgici).
Proscar agisce contro la causa dell'ingrossamento patologico della prostata. Può far ridurre il volume della prostata ingrossata e quindi migliorare i sintomi sopraccitati. Un ingrossamento benigno della prostata si sviluppa su un lungo lasso di tempo, perciò la sua riduzione richiede generalmente una terapia prolungata con Proscar, anche se in qualche caso è stato constatato un rapido miglioramento dei sintomi.
Indipendentemente del fatto che lei osservi un miglioramento o un cambiamento dei sintomi, la terapia con Proscar può ridurre il rischio di una improvvisa ritenzione urinaria oppure di un intervento chirurgico.
Segua i consigli del suo medico. Interrompendo l'uso di Proscar la prostata può di nuovo ingrossarsi ed i sintomi di una iperplasia prostatica benigna possono ricomparire. Consulti regolarmente il suo medico per le visite di controllo. Proscar può influenzare i risultati di un esame del sangue, il cosiddetto test del PSA. Qualora venisse effettuato su di lei il test del PSA, informi il suo medico che sta facendo uso di Proscar.
Quando non si può assumere Proscar?
Non prenda Proscar, se dovesse presentare delle reazioni di ipersensibilità (allergia) verso uno dei componenti.
Proscar non deve essere preso né dalle donne né dai bambini.
Quando è richiesta prudenza nella somministrazione di Proscar?
Informi il suo medico su tutti i problemi medici che ha o ha avuto e su tutte le allergie conosciute che la riguardano.
Se osserva alterazioni nel tessuto della mammella, ad esempio noduli, dolore, ingrossamento o secrezione dai capezzoli, si deve rivolgere immediatamente al suo medico. Queste manifestazioni potrebbero essere il segno di una grave malattia, come il cancro della mammella.
In alcuni uomini in trattamento con Proscar è stata osservata infertilità maschile e/o ridotta qualità dello sperma. È stato tuttavia riferito un miglioramento della qualità dello sperma in seguito all'interruzione dell'assunzione del medicamento.
Le donne in età fertile devono evitare il contatto con Proscar, ad esempio attraverso la manipolazione di compresse rivestite frantumate, in quanto il possibile assorbimento del principio attivo durante la gravidanza può pregiudicare il normale sviluppo degli organi sessuali esterni di bambini di sesso maschile. Le compresse rivestite di Proscar sono protette dal rivestimento, per cui in caso di una normale manipolazione non è possibile il contatto diretto con il principio attivo, a meno che le compresse non vengano schiacciate o frantumate.
Proscar in genere non presenta alcuna interazione con altri medicamenti. Informi comunque sempre il suo medico di tutti i medicamenti che prende al momento o che pensa di prendere, anche di quelli ottenibili senza ricetta.
Informi il suo medico o il suo farmacista nel caso in cui soffre di altre malattie, soffre di allergie o assume o applica esternamente altri medicamenti (anche se acquistati di sua iniziativa)!
Si può assumere Proscar durante la gravidanza o l’allattamento?
Proscar non deve essere assunto dalle donne.
Come usare Proscar?
La dose usuale è di una compressa rivestita di Proscar al giorno, indipendentemente dai pasti.
Prenda Proscar una volta al giorno come prescritto. Se dovesse dimenticare una dose, non prenda una dose extra. Riprenda semplicemente il suo consueto schema di assunzione di una compressa rivestita al giorno.
Se dovesse aver ingerito troppe compresse rivestite in una sola volta, si metta immediatamente in contatto con il suo medico.
Non modifichi di propria iniziativa la posologia prescritta. Se ritiene che l'azione del medicamento sia troppo debole o troppo forte ne parli al suo medico o al suo farmacista (vedi anche il capitolo: «Di che altro occorre tener conto?»).
Quali effetti collaterali può avere Proscar?
I seguenti effetti collaterali possono manifestarsi durante l'assunzione di Proscar:
gli effetti indesiderati osservati frequentemente, e la cui causa era eventualmente, probabilmente o certamente da ricollegare al preparato, sono stati: impotenza, diminuzione della libido (desiderio sessuale) e diminuzione del volume dell'eiaculato.
Durante l'assunzione di Proscar questi effetti indesiderati sono spariti in alcuni casi. Se i sintomi persistono, la situazione si normalizza in genere con l'interruzione dell'assunzione del medicamento.
Occasionalmente, sono stati segnalati effetti indesiderati tra cui disturbi dell'eiaculazione, dolorabilità e/o ingrossamento mammario ed eruzione cutanea.
Raramente, sono stati riportati effetti indesiderati tra cui dolori ai testicoli o reazioni allergiche quali prurito, orticaria, gonfiore delle labbra, della lingua, della gola e del viso.
Se rileva alterazioni del tessuto della mammella, ad esempio noduli, dolore o secrezione dai capezzoli, si deve rivolgere immediatamente al suo medico (vedere «Quando è richiesta prudenza nella somministrazione di Proscar?»).
Sono stati segnalati casi molto rari di cancro della mammella negli uomini.
In casi isolati, sono stati segnalati:
- sangue nello sperma;
- incapacità di erezione, persistente dopo la sospensione del medicamento;
- problemi di eiaculazione, persistenti dopo la sospensione del medicamento;
- riduzione della libido (desiderio sessuale), persistente dopo la sospensione del medicamento;
- depressione.
Anche se osserva effetti collaterali qui non descritti dovrebbe informare il suo medico o il suo farmacista.
Di che altro occorre tener conto?
Indicazione di stoccaggio
A conservare fuori dalla portata dei bambini.
A conservare nella confezione originale, al riparo dalla luce e a temperature inferiori a 30 °C.
Il medicamento non dev'essere utilizzato oltre la data indicata con «EXP» sul contenitore.
Ulteriori indicazioni
Il medico o il farmacista, che sono in possesso di un'informazione professionale dettagliata, possono darle ulteriori informazioni.
Cosa contiene Proscar?
Principi attivi
Una compressa rivestita di Proscar contiene come principio attivo 5 mg di finasteride.
Sostanze ausiliarie
Colorante blu: indigotina (E 132) e altre sostanze ausiliarie.
Numero dell'omologazione
51774 (Swissmedic).
Dov’è ottenibile Proscar? Quali confezioni sono disponibili?
In farmacia, dietro presentazione della prescrizione medica.
Il medicamento è disponibile in confezioni calendario da 28 e 30 o 98 e 105 compresse rivestite.
Titolare dell’omologazione
MSD MERCK SHARP & DOHME AG, Lucerna.
Questo foglietto illustrativo è stato controllato l'ultima volta nel dicembre 2019 dall'autorità competente in materia di medicamenti (Swissmedic).
S-WPPI-MK0906-5T-072018/0906-CHE-2019-021059
Zusammensetzung
Wirkstoff
Finasteridum.
Hilfsstoffe
Color E 132, Excipiens pro compresso obducto.
Darreichungsform und Wirkstoffmenge pro Einheit
Filmtabletten zu 5 mg Finasterid.
Indikationen/Anwendungsmöglichkeiten
Benigne symptomatische Prostatahyperplasie.
Dosierung/Anwendung
Die empfohlene Dosierung beträgt eine Filmtablette Proscar (5 mg Finasterid) täglich unabhängig von den Mahlzeiten.
Spezielle Dosierungsanweisungen
Niereninsuffizienz
Eine Dosisanpassung ist nicht erforderlich, da pharmakokinetische Studien bei Patienten mit fortgeschrittener Niereninsuffizienz (bis hinunter zu einer Kreatinin-Clearance von 9 ml/min/1,73 m²) keinerlei Hinweise auf eine relevante Veränderung der Kinetik von Finasterid erbrachten.
Leberinsuffizienz
Daten bei Leberinsuffizienz sind nicht vorhanden.
Geriatrie
Eine Dosisanpassung ist nicht erforderlich. Die Elimination von Finasterid ist bei über 70-jährigen nur geringfügig vermindert.
Kinder/Jugendliche
Proscar ist bei Kindern und Jugendlichen nicht indiziert.
Kontraindikationen
Proscar ist für Frauen und Kinder nicht indiziert.
Proscar ist kontraindiziert:
- bei Überempfindlichkeit gegenüber irgendeiner Komponente des Präparats.
- bei bestehender oder möglicher Schwangerschaft (siehe «Warnhinweise und Vorsichtsmassnahmen», Finasterid-Exposition und «Schwangerschaft/Stillzeit»).
Warnhinweise und Vorsichtsmassnahmen
Patienten mit grossem Restharnvolumen und/oder stark eingeschränktem Harnfluss sollten sorgfältig auf eine obstruktive Uropathie (akute oder chronische Harnverhaltung) überwacht werden.
Beim Absetzen von Proscar kann sich die Prostata wieder auf die Grösse vor der Behandlung zurückentwickeln. Deshalb sollten die Patienten entsprechend auf das Wiederauftreten von symptomatischer BPH überwacht werden.
Finasterid-Exposition
Proscar Filmtabletten sind beschichtet, wodurch der Kontakt mit dem Wirkstoff bei normaler Handhabung verhindert wird, falls die Filmtabletten nicht zerdrückt oder zerbrochen sind. Frauen sollten keine zerdrückten oder zerbrochenen Proscar Filmtabletten handhaben, wenn sie schwanger sind oder schwanger werden könnten, wegen der möglichen Absorption von Finasterid und des daraus resultierenden möglichen Risikos für einen männlichen Fetus (siehe «Schwangerschaft/Stillzeit»).
Wirkung auf PSA und Prostatakarzinomdetektion
Patienten mit BPH und erhöhten PSA-Werten wurden in kontrollierten klinischen Studien mit wiederholten PSA-Tests und Prostatabiopsien überwacht. In diesen BPH-Studien beeinflusste Proscar die Rate der Prostatakarzinomerkennung nicht. Zwischen Proscar und Placebo gab es in Bezug auf die Gesamtinzidenz von Prostatakarzinomen keinen signifikanten Unterschied.
Es wird empfohlen, vor Therapiebeginn mit Proscar und regelmässig während der Behandlung rektal-digitale Untersuchungen sowie andere Abklärungen zur Erkennung eines Prostatakarzinoms durchzuführen. Auch die Serum-PSA-Bestimmung kann zur Prostatakarzinomerkennung herangezogen werden.
Proscar bewirkt bei Patienten mit BPH eine Abnahme der PSA-Konzentrationen im Serum um ca. 50%, dies auch in Gegenwart eines Prostatakarzinoms. Diese Senkung ist über den gesamten Bereich der PSA-Werte erkennbar, das Ausmass kann individuell variieren. Die Analyse der PSA-Daten von mehr als 3000 Patienten in einer doppelblinden, placebo-kontrollierten 4-Jahres-Studie (PLESS) bestätigte, dass bei Patienten, die 6 Monate oder länger mit Proscar behandelt wurden, die während der Behandlung mit Proscar gemessenen PSA-Werte für den Vergleich mit den Normwerten unbehandelter Männer mit 2 multipliziert werden müssen. Auf diese Weise können Sensitivität und Spezifizität des PSA-Assays zur Erkennung eines Prostatakarzinoms trotz der Finasterid-Behandlung aufrechterhalten werden.
Jegliche andauernde Erhöhung von PSA-Werten bei Patienten unter Therapie mit Proscar sollte sorgfältig evaluiert werden, einschliesslich der Möglichkeit fehlender Compliance im Hinblick auf die Behandlung mit Proscar.
Das Verhältnis von freiem zu Gesamt-PSA bleibt auch unter dem Einfluss von Proscar konstant. Wenn der Prozentanteil von freiem PSA zur Erkennung eines Prostatakarzinoms verwendet wird, ist keine Anpassung des Wertes notwendig.
Prostatakarzinom
Bei Patienten mit Prostatakarzinom, welche mit Finasterid behandelt wurden, wurde bis heute kein klinischer Nutzen beobachtet.
In einer placebo-kontrollierten 7jährigen Studie an 18'882 gesunden Männern mit einem Mindestalter von 55 Jahren, normalem rektal-digitalem Befund und PSA Werten von ≤3.0 ng/ml, wurde bei insgesamt 9060 auswertbaren Prostatabiopsien unter Behandlung mit Finasterid 5 mg in 18,4%, unter Placebo in 24,4% ein Prostatakarzinom diagnostiziert. In der Finasteridgruppe war die Diagnose eines Prostatakarzinoms mit höherem histologischem Grad (Gleason Score 7-10) häufiger als in der Placebogruppe (6,4% vs. 5,1%). Über einen möglichen Kausalzusammenhang zwischen Finasterid und Karzinomen mit höherem histologischem Grad ist bisher keine Aussage möglich.
Mammakarzinom bei Männern
In sehr seltenen Fällen wurde in klinischen Studien sowie nach Markteinführung unter Finasterid 5 mg ein Mammakarzinom bei Männern beobachtet. Über einen Kausalzusammenhang zwischen der Langzeitanwendung von Finasterid und Mammakarzinomen beim Mann ist derzeit keine Aussage möglich. Ärzte sollten ihre Patienten anweisen, unverzüglich jegliche Veränderungen des Brustgewebes wie Knoten, Schmerzen, Gynäkomastie oder Sekretion aus der Brustwarze zu berichten.
Fertilität
Es liegen Berichte über männliche Infertilität bzw. eine reduzierte Spermienqualität unter Behandlung mit 5α-Reduktasehemmern vor. Nach Absetzen von Finasterid wurde über eine Normalisierung bzw. Verbesserung der reduzierten Spermienqualität berichtet (vgl. auch «Eigenschaften/Wirkungen», Sicherheitspharmakodynamik).
Interaktionen
Beim Menschen wurden Propranolol, Digoxin, Glibenclamid, Warfarin, Theophyllin und Phenazon auf ihre möglichen Interaktionen mit Proscar überprüft. Dabei wurden keine klinisch bedeutsamen Wechselwirkungen beobachtet. Es gibt keine Hinweise darauf, dass Proscar die arzneistoffmetabolisierenden Enzyme des Cytochrom-P450-Systems beeinträchtigt.
Andere gleichzeitige Behandlungen
Obschon keine spezifischen Interaktions-Studien durchgeführt wurden, wurde Proscar in klinischen Studien gleichzeitig mit ACE-Inhibitoren, Acetaminophen, Acetylsalicylsäure, Alpha-Blockern, Beta-Blockern, Calcium-Antagonisten, Nitraten, Diuretika, H2-Antagonisten, HMG-CoA- Reduktase-Inhibitoren, nichtsteroidalen Entzündungshemmern (NSAR), Chinolonen und Benzodiazepinen ohne Hinweis auf klinisch relevante Interaktionen verabreicht.
Schwangerschaft/Stillzeit
Es gibt keine Indikation für Proscar bei Frauen. Wird von einer Schwangeren Proscar eingenommen, könnte es aufgrund des Wirkmechanismus bei einem männlichen Fetus zu Anomalien der äusseren Geschlechtsorgane kommen (siehe «Warnhinweise und Vorsichtsmassnahmen», Finasterid-Exposition und «Präklinische Daten»).
Da Proscar bei Frauen nicht indiziert ist, ist nicht bekannt, ob Finasterid in die Muttermilch übergeht.
Zur Übertragung von Finasterid aus dem Sperma auf den Fetus liegen keine Humandaten vor (siehe «Präklinische Daten»).
Wirkung auf die Fahrtüchtigkeit und auf das Bedienen von Maschinen
Entsprechende Studien wurden nicht durchgeführt. Es gibt jedoch keine Hinweise darauf, dass Proscar die Fahrtüchtigkeit oder das Bedienen von Maschinen beeinträchtigt.
Unerwünschte Wirkungen
Die Angaben zur Sicherheit von Proscar basieren schwerpunktmässig auf der PLESS-Studie (Placebo-kontrollierte Studie mit vierjähriger Behandlungsdauer an n=3040 Patienten). Über folgende unerwünschte Wirkungen wurde in klinischen Studien mit Proscar und/oder nach Markteinführung von Proscar und/oder unter Finasterid in niedrigeren Dosierungen berichtet. Da Ereignisse nach Markteinführung aus einer Population unbekannter Grösse und auf freiwilliger Basis gemeldet werden, kann deren Häufigkeit oder Kausalzusammenhang mit dem Arzneimittel nicht immer zuverlässig eingeschätzt werden.
Sehr häufig (≥1/10), häufig (≥1/100, <1/10), gelegentlich (≥1/1000, <1/100), selten (≥1/10'000, <1/1000), sehr selten (<1/10'000), unbekannt (überwiegend auf Spontanmeldungen aus der Marktüberwachung beruhend, Häufigkeit kann aus den vorhandenen Daten nicht abgeschätzt werden).
Erkrankungen des Immunsystems
Selten: Überempfindlichkeitsreaktionen, wie Angioödem (einschliesslich Schwellung von Lippen, Zunge, Rachen oder Gesicht).
Psychiatrische Erkrankungen
Häufig: verminderte Libido.
Unbekannt: Depression; verminderte Libido, nach Absetzen der Behandlung fortbestehend
Erkrankungen der Haut und des Unterhautzellgewebes
Gelegentlich: Hautausschlag.
Selten: Pruritus, Urtikaria.
Erkrankungen der Geschlechtsorgane und der Brustdrüse
Häufig: Impotenz, verringerte Ejakulatmenge.
Gelegentlich: Ejakulationsstörungen, Brustvergrösserung, Brustempfindlichkeit.
Selten: Hodenschmerzen.
Unbekannt: persistierende sexuelle Dysfunktion (erektile Dysfunktion und Ejakulationsstörungen) nach Absetzen der Behandlung; Hämatospermie.
Basierend auf dem Profil der unerwünschten Wirkungen von PLESS, den einjährigen placebo-kontrollierten Phase III Studien und den 5-Jahres-Extensionen, einschliesslich 853 Patienten, welche über 5-6 Jahre behandelt wurden, gibt es keine Hinweise auf vermehrte unerwünschte Wirkungen bei längerer Behandlungsdauer mit Proscar. Die Inzidenz von neuen arzneimittelbezogenen unerwünschten Wirkungen auf die Sexualfunktion nahm mit der Dauer der Behandlung ab.
In sehr seltenen Fällen wurde über ein Mammakarzinom beim Mann berichtet (siehe «Warnhinweise und Vorsichtsmassnahmen»).
Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von grosser Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdacht einer neuen oder schwerwiegenden Nebenwirkung über das Online-Portal ElViS (Electronic Vigilance System) anzuzeigen. Informationen dazu finden Sie unter www.swissmedic.ch.
Überdosierung
Einzeldosen bis zu 400 mg Finasterid und fortgesetzte Verabreichung von bis zu 80 mg täglich über 3 Monate blieben beim Menschen ohne Nebenwirkungen.
Es existiert kein spezifisches Antidot für Finasterid. Eine Überdosierung sollte ggf. symptomatisch behandelt werden.
Eigenschaften/Wirkungen
ATC-Code: G04CB01
Wirkungsmechanismus
Finasterid, ein synthetisches 4-Azasteroid, ist ein spezifischer, kompetitiver Hemmer der Typ-II 5 α-Reduktase, eines intrazellulären Enzyms, welches die Umwandlung von Testosteron zum wirksameren Androgen Dihydrotestosteron (DHT) katalysiert. Bei der benignen Prostatahyperplasie (BPH) ist die Vergrösserung der Prostata abhängig von der Umwandlung von Testosteron zu DHT innerhalb der Prostata. Proscar reduziert das zirkulierende und das intraprostatische DHT. Finasterid hat keine Affinität zum Androgen-Rezeptor.
Proscar behandelt und kontrolliert die Symptome der benignen Prostatahyperplasie (BPH) und senkt das Risiko eines akuten Harnverhaltes sowie den Bedarf für operative Eingriffe (wie transurethrale Resektion der Prostata (TURP) oder Prostatektomie). Proscar verkleinert die vergrösserte Prostata und verbessert Harnfluss und BPH-assoziierte Symptome.
Pharmakodynamik
Sicherheitspharmakodynamik
Zur Beurteilung von Sperma-Parametern erhielten n=138 gesunde Probanden 5 mg Finasterid/Tag über 24 Wochen. Konzentration, Mobilität und Morphologie der Spermien sowie der pH-Wert wurden nicht in klinisch relevanter Weise beeinflusst. Das Ejakulatvolumen nahm im Median um 0,6 ml ab bei einer gleichzeitigen Reduktion der Gesamtzahl der Spermien pro Ejakulat. Diese Parameter blieben innerhalb des Normbereiches und erreichten nach Beendigung der Therapie wieder die Ausgangswerte.
Klinische Wirksamkeit
In der Proscar Langzeit- und Sicherheitsstudie (PLESS) wurde die Wirkung der Therapie mit Proscar auf BPH-bedingte urologische Ereignisse (operative Eingriffe [transurethrale Resektion der Prostata bzw. Prostatektomie] oder Katheterisierung nach akuter Harnverhaltung) über 4 Jahre an 3016 Patienten mit mittleren bis schweren BPH-Symptomen ermittelt. In dieser doppelblinden, randomisierten, placebokontrollierten Multizenter-Studie reduzierte die Behandlung mit Proscar das Risiko aller urologischen Ereignisse um 51% und war mit einer deutlichen und andauernden Regression des Prostatavolumens, einer anhaltenden Steigerung der maximalen Harnflussrate und einer Verbesserung der Symptome assoziiert.
Eine Meta-Analyse der Ein-Jahres-Daten von 7 doppelblinden, placebo-kontrollierten Studien vergleichbaren Designs, die insgesamt 4491 Patienten mit symptomatischer BPH umfassten, zeigte, dass die Symptomverbesserung und der Grad der Verbesserung der Harnflussrate ausgeprägter war bei Patienten unter Proscar, deren Prostata zum Zeitpunkt des Studienbeginns vergrössert war (ca. 40 cc und grösser) gegenüber Patienten mit geringerem Prostatavolumen. Diese Studiendaten zeigen, dass Proscar die Progression der BPH bei Männern mit einer vergrösserten Prostata rückgängig macht.
Pharmakokinetik
Absorption
Die absolute Bioverfügbarkeit von Finasterid beträgt etwa 80% und wird durch Nahrungszufuhr nicht beeinflusst. Maximale Plasmakonzentrationen von Finasterid werden ca. zwei Stunden nach Einnahme erreicht, die Resorption ist nach 6 - 8 Stunden abgeschlossen.
Steady State-Bedingungen: Eine Mehrfachdosis-Studie zeigte eine langsame Akkumulierung kleinster Mengen von Finasterid. Bei einer täglichen Dosis von 5 mg betragen die Steady-state Plasma-Konzentrationen ca. 8-10 ng/ml und bleiben stabil.
Die maximale Plasma-Konzentration (Cmax) bei einer täglichen Dosis von 5 mg betrug für 45- bis 60-jährige Patienten 46,2 ng/ml, für 70-jährige Patienten 48,4 ng/ml.
Die minimale Plasma-Konzentration (Cmin) bei einer täglichen Dosis von 5 mg betrug für 45- bis 60-jährige Patienten 6,2 ng/ml, für 70-jährige Patienten 8,1 ng/ml.
Distribution
Die Proteinbindung von Finasterid beträgt ca. 93%, das Verteilungsvolumen ungefähr 76 Liter.
Finasterid konnte in der Samenflüssigkeit von Probanden nachgewiesen werden, welche Proscar 5 mg/Tag erhalten hatten. Die Menge von Finasterid in der Samenflüssigkeit entspricht weniger als 1/50 - 1/100 einer Finasterid Dosis (5 μg), die keinen Effekt auf die zirkulierenden DHT-Spiegel bei Männern hatte.
Obwohl bei Männern, die über 7 bis 10 Tage mit Finasterid behandelt wurden, Finasterid auch im Liquor nachgewiesen werden konnte, scheint sich die Substanz dort nicht präferentiell zu konzentrieren.
Metabolismus
Finasterid wird extensiv in der Leber metabolisiert, hauptsächlich via Enzyme der Cytochrom-P450 3A4-Subfamilie. Zwei Metaboliten wurden identifiziert, welche nur einen Bruchteil der inhibitorischen Aktivität von Finasterid auf die 5α-Reduktase besitzen.
Elimination
Die durchschnittliche Plasma-Eliminations-Halbwertszeit von Finasterid beträgt sechs Stunden, die Plasma-Clearance ca. 165 ml/min.
Nach oraler Verabreichung von 14C-Finasterid wurden 39% der Dosis mit dem Urin in Form von Metaboliten und 57% der Gesamtdosis mit den Faezes ausgeschieden. Im Urin fand sich praktisch kein unverändertes Finasterid.
Kinetik spezieller Patientengruppen
Ältere Patienten: Mit zunehmendem Alter verringert sich die Eliminationsrate geringfügig, und die Halbwertszeit verlängert sich von einem Durchschnittswert von ca. sechs Stunden bei 18- bis 60-jährigen auf ca. acht Stunden bei über 70-jährigen Männern. Diese Befunde sind ohne klinische Relevanz.
Niereninsuffizienz: Bei Patienten mit einer Kreatinin-Clearance zwischen 9 und 55 ml/min/1,73 m2 war die Pharmakokinetik einer Einzeldosis von 14C- Finasterid jener bei gesunden Probanden vergleichbar. Auch bei der Proteinbindung gab es keine Unterschiede. Ein Teil der Metaboliten, die normalerweise mit dem Urin ausgeschieden werden, wurde mit den Faezes ausgeschieden. Die vermehrte Ausscheidung über die Faezes kompensiert offenbar die verminderte Ausscheidung der Metaboliten über die Nieren.
Leberinsuffizienz: Daten bei Leberinsuffizienz liegen nicht vor.
Präklinische Daten
Die pränatale Finasterid-Exposition während der Organogenese führte bei der männlichen Ratte der F-1 Generation zu verkürztem Anogenitalabstand, Missbildungen der externen Genitalien, Hypospadien, transienten Mamillen und zur Abnahme des Prostatagewichts.
Die intravenöse Verabreichung von Finasterid bei graviden Rhesusaffen in so hohen Dosen wie 800 ng/d während der gesamten Zeit der embryonalen und foetalen Entwicklung ergab bei männlichen Foeten keine Missbildungen. Die Exposition unter dieser Dosis ist mindestens 60-120 mal höher als jene, welche bei schwangeren Frauen geschätzt wurde im Falle eines Kontaktes mit Samenflüssigkeit von Männern, die 5mg/d einnehmen. Als Bestätigung der Relevanz des Rhesusmodells für die Entwicklung des menschlichen Foeten hatte die orale Verabreichung einer sehr hohen Dosis von Finasterid (2 mg/kg/d; dies entspricht dem 20-fachen der empfohlenen Dosis 5mg/d für den Menschen oder dem ungefähr 1-2-Millionenfachen der höchsten Schätzung bezüglich der Finasterid-Exposition durch Samenflüssigkeit) bei graviden Affen Missbildungen am äusseren Genitale männlicher Foeten zu Folge. Andere Missbildungen bei männlichen Foeten oder Finasterid-bedingte Missbildungen bei weiblichen Foeten wurden bei keiner Dosierung des Arzneimittels beobachtet.
Sonstige Hinweise
Beeinflussung diagnostischer Methoden
Bei der Beurteilung von PSA-Werten ist zu beachten, dass diese bei Patienten, welche mit Proscar behandelt werden, erniedrigt sind (siehe «Warnhinweise und Vorsichtsmassnahmen», Wirkung auf PSA und Prostatakarzinomdetektion).
Haltbarkeit
Das Arzneimittel darf nur bis zu dem auf der Packung mit «EXP» bezeichneten Datum verwendet werden.
Besondere Lagerungshinweise
Für Kinder unerreichbar aufbewahren.
In der Originalverpackung vor Licht geschützt bei unter 30 °C aufbewahren.
Zulassungsnummer
51774 (Swissmedic).
Zulassungsinhaberin
MSD MERCK SHARP & DOHME AG, Luzern.
Stand der Information
Dezember 2019
S-IPC-MK0906-5T-072018/0906-CHE-2019-021059
Composition
Principe actif
Finasteridum.
Excipients
Colorant E 132, Excipiens pro compresso obducto.
Forme pharmaceutique et quantité de principe actif par unité
Comprimés pelliculés à 5 mg de finastéride.
Indications/Possibilités d’emploi
Hyperplasie bénigne de la prostate symptomatique.
Posologie/Mode d’emploi
La posologie recommandée est d'un comprimé pelliculé de Proscar (5 mg de finastéride) par jour, indépendamment des repas.
Instructions posologiques particulières
Insuffisance rénale
Une adaptation de la posologie n'est pas nécessaire chez les patients souffrant d'insuffisance rénale avancée (jusqu'à une clairance de la créatinine de 9 ml/min/1,73 m²), étant donné que des études pharmacocinétiques n'ont montré aucune modification significative de la cinétique du finastéride.
Insuffisance hépatique
On ne dispose pas de données concernant l'insuffisance hépatique.
Patients âgés
Aucune adaptation de posologie n'est requise. L'élimination du finastéride n'est que légèrement diminuée chez les patients âgés de plus de 70 ans.
Enfants/adolescents
Proscar n'est pas indiqué pour le traitement des enfants ou des adolescents.
Contre-indications
Proscar n'est pas indiqué chez les femmes et les enfants.
Proscar est contre-indiqué:
- lors d'hypersensibilité à l'un des composants du médicament;
- en cas de grossesse confirmée ou possible (voir sous «Mises en garde et précautions», Exposition au finastéride et «Grossesse/Allaitement»).
Mises en garde et précautions
Chez les patients dont le volume urinaire résiduel est important et/ou dont le débit urinaire est fortement diminué, l'éventuelle apparition d'une uropathie obstructive (rétention urinaire aiguë ou chronique) doit être surveillée attentivement.
Lorsque le traitement avec Proscar est arrêté, le volume de la prostate peut revenir à celui d'avant le traitement. C'est pourquoi il convient de rester attentif à une éventuelle réapparition d'une HBP symptomatique.
Exposition au finastéride:
Les comprimés pelliculés de Proscar sont recouverts d'un film, ce qui empêche tout contact avec le principe actif lors des manipulations usuelles, à condition que les comprimés pelliculés ne soient pas cassés ou écrasés. Les femmes enceintes ou susceptibles de l'être ne doivent pas manipuler les comprimés pelliculés de Proscar cassés ou écrasés, en raison de l'absorption possible du finastéride par la peau et le risque potentiel qui s'ensuit pour le fœtus du sexe masculin (voir sous «Grossesse/Allaitement»).
Effet sur le PSA et le dépistage du cancer de la prostate:
Des patients atteints d'HBP et présentant des valeurs élevées de PSA ont été surveillés au cours d'études cliniques contrôlées à l'aide de tests répétés de PSA et de biopsies de la prostate. Dans le cadre de ces études, Proscar n'a pas eu d'influence sur le taux de dépistage des cancers de la prostate. Aucune différence significative concernant l'incidence totale de cancers de la prostate entre Proscar et le placebo n'a été constatée.
Il est recommandé de pratiquer un toucher rectal ainsi que d'autres examens destinés au dépistage d'un cancer de la prostate avant l'instauration du traitement et périodiquement par la suite. La détermination du PSA sérique peut également contribuer à l'identification d'un cancer de la prostate.
Chez des patients atteints d'une HBP, Proscar provoque une diminution de 50% environ des concentrations sériques de PSA, également en présence d'un cancer de la prostate. Cette diminution se manifeste sur toute la gamme des valeurs de PSA, bien que son ampleur puisse varier d'un patient à l'autre. L'analyse des données de PSA provenant de plus de 3000 patients, issues d'une étude de 4 ans menée en double aveugle, contrôlée par placebo (PLESS), a confirmé que chez les patients traités avec Proscar pendant 6 mois ou plus, les valeurs de PSA mesurées pendant le traitement avec Proscar doivent être multipliées par deux pour pouvoir être comparées aux valeurs normales chez les hommes non traités. Cette manière de procéder permet de maintenir la sensibilité et la spécificité de l'analyse PSA pour le dépistage d'un cancer de la prostate malgré le traitement par finastéride.
Il faut examiner soigneusement toute élévation durable de la concentration sérique de PSA chez les patients traités par Proscar, en considérant la possibilité d'une mauvaise observance du traitement par Proscar.
Le rapport entre le PSA libre et le PSA total reste également constant sous l'effet de Proscar. Lorsque le pourcentage de PSA libre est utilisé pour le dépistage d'un cancer de la prostate, aucun ajustement de la valeur n'est nécessaire.
Cancer de la prostate
Chez les patients atteints d'un cancer prostatique qui ont été traités au finastéride, aucun bénéfice clinique n'a été observé à ce jour.
Dans une étude de 7 ans contrôlée par placebo, effectuée auprès de 18'882 hommes sains âgés d'au moins 55 ans qui présentaient des résultats normaux au toucher rectal ainsi que des taux de PSA ≤3,0 ng/ml, on a obtenu au total 9060 biopsies analysables de la prostate qui ont permis de diagnostiquer un cancer de la prostate dans 18,4% des cas sous finastéride 5 mg et 24,4% des cas sous placebo. Les cancers présentant un grade histologique plus élevé (scores de Gleason de 7 à 10) ont été plus fréquents dans le groupe sous finastéride que dans le groupe sous placebo (6,4% vs 5,1%). Aucune affirmation n'est possible à ce jour sur un éventuel rapport causal entre le finastéride et les cancers de grade histologique plus élevé.
Cancer du sein chez l'homme
Dans le cadre d'études cliniques et après la commercialisation, un cancer du sein a été observé dans de très rares cas chez des hommes traités au finastéride 5 mg. Aucune affirmation n'est actuellement possible sur un éventuel rapport causal entre l'utilisation prolongée de finastéride et le développement d'un cancer du sein chez l'homme. Les médecins doivent instruire leurs patients de signaler immédiatement toute survenue de modifications du tissu mammaire telles que par exemple nodules, douleurs, gynécomastie ou sécrétions du mamelon.
Fertilité
Il existe des rapports d'infertilité masculine ou de qualité réduite du sperme sous inhibiteurs de la 5α-réductase. Une normalisation/amélioration de la qualité réduite du sperme a été rapportée après l'arrêt de l'administration du finastéride (voir «Propriétés/Effets», Pharmacodynamique).
Interactions
Proscar a été testé chez l'homme en ce qui concerne de possibles interactions avec le propranolol, la digoxine, le glibenclamide, la warfarine, la théophylline et la phénazone. Aucune interaction cliniquement significative n'a été observée. Rien n'indique que Proscar puisse affecter les enzymes du système du cytochrome P450 impliquées dans le métabolisme des médicaments.
Autres traitements concomitants:
Bien qu'aucune interaction n'ait été étudiée spécifiquement, Proscar a déjà été administré au cours d'études cliniques en même temps que les produits ci-après, sans qu'une interaction cliniquement significative n'ait été mise en évidence: inhibiteurs de l'ECA, acétaminophène, acide acétylsalicylique, alpha-bloquants, bêta-bloquants, antagonistes du calcium, dérivés nitrés, diurétiques, antagonistes des récepteurs H2, inhibiteurs de la HMG-CoA-réductase, anti-inflammatoires non-stéroïdiens (AINS), quinolones et benzodiazépines.
Grossesse/Allaitement
Il n'existe pas d'indication de Proscar pour les femmes. En cas d'administration de Proscar à une femme enceinte, des anomalies au niveau des organes génitaux externes d'un fœtus mâle pourraient survenir en raison du mécanisme d'action du produit (voir sous «Mises en garde et précautions», Exposition au finastéride et «Données précliniques»).
En raison de l'absence d'indication de Proscar chez les femmes, on ignore si le finastéride passe dans le lait maternel.
On ne dispose d'aucune donnée sur le passage du finastéride à partir de sperme au fœtus de l'être humain (voir sous «Données précliniques»).
Effet sur l’aptitude à la conduite et l’utilisation de machines
Aucune étude correspondante n'a été effectuée. Il n'existe toutefois aucun indice laissant supposer que Proscar diminue la capacité à conduire des véhicules ou à utiliser des machines.
Effets indésirables
Les informations sur la sécurité de Proscar reposent essentiellement sur l'étude PLESS (une étude contrôlée par placebo, d'une durée de 4 ans, auprès de n=3040 patients). Les effets indésirables ci-après ont été rapportés dans les études cliniques sur Proscar et/ou après la commercialisation de Proscar et/ou sous finastéride faiblement dosé. Étant donné que les rapports d'événements survenus après la commercialisation sont spontanés et proviennent d'une population de taille inconnue, leur fréquence ou leur lien de causalité avec le médicament ne peuvent pas toujours être estimés de façon fiable.
Très fréquents (≥1/10), fréquents (≥1/100, <1/10), occasionnels (≥1/1000, <1/100), rares (≥1/10'000, <1/1000), très rares (<1/10'000), fréquence inconnue (essentiellement sur la base de rapports spontanés dans le cadre de la surveillance du marché, dont les données disponibles ne permettent pas d'estimer la fréquence).
Affections du système immunitaire
Rares: réactions d'hypersensibilité telles qu'angio-œdème (y compris gonflement des lèvres, de la langue, du pharynx ou du visage).
Affections psychiatriques
Fréquent: baisse de la libido.
Fréquence inconnue: dépression, baisse de la libido, persistant après l'arrêt du traitement.
Affections de la peau et du tissu sous-cutané
Occasionnel: éruption cutanée.
Rares: prurit, urticaire.
Affections des organes de reproduction et du sein
Fréquents: impuissance sexuelle, diminution du volume d'éjaculat.
Occasionnels: troubles de l'éjaculation, gonflement mammaire, sensibilité douloureuse des seins.
Rares: douleurs testiculaires.
Fréquence inconnue: dysfonction sexuelle persistante (dysfonction érectile et troubles de l'éjaculation) après l'arrêt du traitement; hématospermie.
Sur la base du profil d'effets indésirables observé dans l'étude PLESS, dans les études de phase III contrôlées par placebo d'une durée d'un an, et des études d'extension de 5 ans, y compris de 853 patients traités pendant 5 à 6 ans, il n'existe aucun indice d'une augmentation des effets indésirables lors d'une durée prolongée du traitement par Proscar. L'incidence des effets indésirables nouveaux observés en rapport avec le médicament sur la fonction sexuelle a régressé sur la durée du traitement.
De très rares cas de cancer du sein chez l'homme ont été rapportés (voir «Mises en garde et précautions»).
L'annonce d'effets secondaires présumés après l'autorisation est d'une grande importance. Elle permet un suivi continu du rapport bénéfice-risque du médicament. Les professionnels de santé sont tenus de déclarer toute suspicion d'effet secondaire nouveau ou grave via le portail d'annonce en ligne ElViS (Electronic Vigilance System). Vous trouverez des informations à ce sujet sur www.swissmedic.ch.
Surdosage
Des doses uniques de finastéride pouvant aller jusqu'à 400 mg et des doses répétées pouvant aller jusqu'à 80 mg/jour pendant 3 mois n'ont pas provoqué d'effet secondaire chez l'homme.
Il n'existe aucun antidote spécifique contre le finastéride. Un surdosage doit éventuellement être traité de façon symptomatique.
Propriétés/Effets
Code ATC: G04CB01
Mécanisme d'action
Le finastéride, un 4-azastéroïde de synthèse, est un inhibiteur spécifique et compétitif de la 5α-réductase de type II, une enzyme intracellulaire catalysant la transformation de la testostérone en un androgène plus actif, la dihydrotestostérone (DHT). Lors de l'hyperplasie bénigne de la prostate (HBP), l'augmentation du volume de la prostate dépend de la transformation de testostérone en DHT à l'intérieur de la prostate. Proscar fait chuter la DHT circulante et intraprostatique. Le finastéride n'a pas d'affinité pour le récepteur androgénique.
Proscar traite et contrôle les symptômes de l'hyperplasie bénigne de la prostate (HBP) et diminue le risque de rétention urinaire aiguë ainsi que le besoin d'interventions chirurgicales (telles que résection transuréthrale de la prostate (RTUP) ou prostatectomie). Proscar réduit le volume de la prostate agrandie et améliore le flux urinaire et les symptômes associés à l'HBP.
Pharmacodynamique
Pharmacodynamique de sécurité
Pour l'évaluation des paramètres du sperme, n=138 sujets sains ont reçu du finastéride à raison de 5 mg par jour pendant 24 semaines. Aucune influence cliniquement significative n'a été constatée sur la concentration des spermatozoïdes, leur mobilité ou leur morphologie, ni sur le pH du sperme. On a constaté une réduction médiane de 0,6 ml du volume d'éjaculat en même temps qu'une réduction du nombre total de spermatozoïdes par éjaculat. Ces paramètres sont toutefois restés dans les limites de la normale et sont revenus aux valeurs initiales après la fin du traitement.
Efficacité clinique
L'étude de longue durée sur la sécurité (PLESS) a permis de déterminer l'effet du traitement avec Proscar sur les événements urologiques dus à l'HBP (interventions chirurgicales [résection transuréthrale de la prostate ou prostatectomie] ou cathétérisme après une rétention urinaire aiguë) pendant 4 ans chez 3016 patients souffrant de symptômes liés à l'HBP d'intensité modérée à sévère. Cette étude menée en double aveugle, randomisée, contrôlée par placebo, multicentrique a montré qu'un traitement avec Proscar réduit le risque de tous les événements urologiques de 51% et que ce traitement a pu être mis en relation avec une diminution nette et durable du volume de la prostate, une élévation persistante du flux urinaire maximal et une amélioration des symptômes.
Une méta-analyse des données d'un an issues de 7 études menées en double aveugle contrôlées par placebo, de conception comparable, impliquant un total de 4491 patients atteints d'HBP symptomatique, a montré que dans les groupes traités par Proscar, l'amélioration des symptômes et le degré de l'amélioration du flux urinaire étaient plus marqués chez les patients dont le volume prostatique était plus élevé au moment de l'entrée dans l'étude (environ 40 cc et plus) que chez les patients dont le volume prostatique était plus faible. Ces résultats d'étude montrent que Proscar fait régresser l'HBP chez les hommes avec une prostate agrandie.
Pharmacocinétique
Absorption
La biodisponibilité absolue du finastéride est d'environ 80% et n'est pas modifiée par la prise simultanée d'aliments. Les concentrations plasmatiques maximales du finastéride sont atteintes approximativement 2 heures après administration orale et l'absorption est complète après 6 à 8 heures.
Conditions à l'état d'équilibre:
Une étude avec des doses multiples a montré une lente accumulation de très faibles quantités de finastéride. Après une administration quotidienne de 5 mg par jour, à l'état d'équilibre, les concentrations plasmatiques de finastéride varient entre 8 et 10 ng/ml et restent stables.
Les concentrations plasmatiques maximales (Cmax) après une prise quotidienne de 5 mg étaient de 46,2 ng/ml chez les patients âgés de 45 à 60 ans et de 48,4 ng/ml chez les patients de 70 ans.
Les concentrations plasmatiques minimales (Cmin) après une prise quotidienne de 5 mg étaient de 6,2 ng/ml chez les patients âgés de 45 à 60 ans et de 8,1 ng/ml chez les patients de 70 ans.
Distribution
La liaison aux protéines plasmatiques est d'environ 93%. Le volume de distribution du finastéride est de 76 litres environ. Du finastéride a été retrouvé dans le liquide séminal de volontaires ayant reçu 5 mg de Proscar par jour. La quantité de finastéride dans le liquide séminal correspond à moins de 1/50 - 1/100 d'une dose de finastéride (5 μg), qui n'a pas eu d'effet sur le taux de DHT circulante chez les hommes.
Bien que le finastéride ait été retrouvé également dans le liquide céphalo-rachidien de patients traités pendant 7 à 10 jours au finastéride, il ne semble pas s'y concentrer préférentiellement.
Métabolisme
Le finastéride est métabolisé de façon extensive dans le foie, principalement par les enzymes de la sous-famille 3A4 du cytochrome P450. On a identifié deux métabolites qui ne possèdent qu'une faible fraction de l'activité inhibitrice du finastéride sur la 5α-réductase.
Élimination
La demi-vie moyenne d'élimination plasmatique du finastéride est de 6 heures et la clairance plasmatique est d'environ 165 ml/min.
Après administration orale de 14C-finastéride, 39% de la dose sont excrétés dans les urines sous forme de métabolites et 57% de la dose totale sont excrétés dans les fèces. Pratiquement aucun finastéride inchangé n'a été retrouvé dans les urines.
Cinétique pour certains groupes de patients
Patients âgés: Le taux d'élimination du finastéride diminue discrètement avec l'âge: la demi-vie, d'environ 6 heures entre 18 et 60 ans, s'allonge jusqu'à 8 heures après 70 ans. Ceci n'a pas de conséquences cliniques.
Insuffisance rénale: Chez les patients avec une clairance de la créatinine comprise entre 9 et 55 ml/min/1,73 m², la pharmacocinétique d'une dose unique de 14C-finastéride était comparable à celle de volontaires sains. Aucune différence n'a non plus été constatée en ce qui concerne la liaison aux protéines plasmatiques. Une partie des métabolites qui est normalement excrétée par voie rénale, est excrétée dans les fèces. Il semble donc que l'excrétion fécale plus élevée compense la diminution de l'excrétion urinaire des métabolites.
Insuffisance hépatique: On ne dispose pas de données concernant l'insuffisance hépatique.
Données précliniques
L'exposition prénatale au finastéride pendant l'organogènese provoque chez le rat de sexe masculin de la génération F-1 une distance ano-génitale plus courte, des malformations des organes génitaux externes, des hypospadias, des mamelons transitoires et une diminution de la masse de la prostate.
L'administration de finastéride par voie intraveineuse à des singes rhésus femelles gravides à des doses élevées allant jusqu'à 800 ng/jour pendant toute la période du développement embryonnaire et fœtal n'a pas provoqué de malformation chez les fœtus mâles. L'exposition atteinte sous cette dose est au moins 60 à 120 fois supérieure à celle estimée chez la femme enceinte dans le cas d'un contact avec le sperme d'hommes ayant pris la dose de 5 mg/jour. Afin de confirmer la pertinence du modèle du singe rhésus pour le développement du fœtus humain, il a été démontré que l'administration par voie orale d'une dose très élevée de finastéride (2 mg/kg/jour; cette dose correspond à 20 fois la dose recommandée de 5 mg/jour chez l'homme ou à près de 1 à 2 millions de fois la valeur évaluée la plus élevée en termes d'exposition au finastéride par le sperme) à des singes femelles en gestation provoque des malformations des organes génitaux externes de fœtus mâles. Aucune autre malformation n'a été observée chez des fœtus du sexe masculin et aucune malformation due au finastéride n'a été constatée chez des fœtus du sexe féminin, quelle que soit la posologie du médicament.
Remarques particulières
Influence sur les méthodes de diagnostic
Lors de l'analyse des valeurs du PSA, il faut tenir compte du fait qu'elles sont abaissées chez les patients traités par Proscar (voir sous «Mises en garde et précautions», Effet sur le PSA et le dépistage du cancer de la prostate).
Stabilité
Le médicament ne doit pas être utilisé au-delà de la date figurant après la mention «EXP» sur l'emballage.
Remarques particulières concernant le stockage
Tenir hors de la portée des enfants.
A conserver dans l'emballage d'origine, à l'abri de la lumière et à une température inférieure à 30 °C.
Numéro d’autorisation
51774 (Swissmedic).
Titulaire de l’autorisation
MSD MERCK SHARP & DOHME AG, Lucerne.
Mise à jour de l’information
Décembre 2019
S-IPC-MK0906-5T-072018/0906-CHE-2019-021059
Відгуки (0)
Ви переглядали

Безкоштовна консультація досвідченого спеціаліста
Опишіть симптоми або потрібний продукт - ми допоможемо підібрати його дозування або аналог, оформити замовлення з доставкою додому або просто проконсультуємо.
Нас 14 спеціалістів і 0 ботів. Ми завжди будемо з вами на зв'язку і зможемо зв'язатися в будь-який час.




 Deutsch
Deutsch French
French Italian
Italian