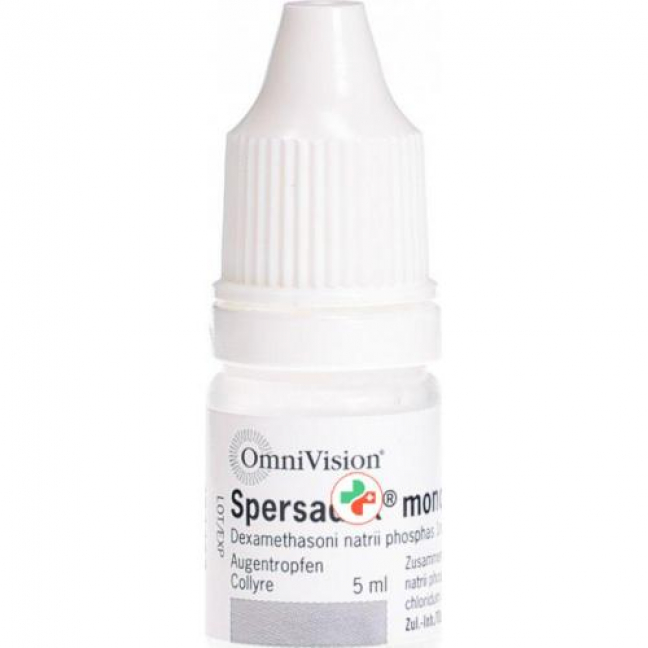
Сперсадекс моно Gtt Opht 0,1% Fl 5 мл
Spersadex Mono 0.1% 5 ml
-
4661.91 RUB
Дата доставки:
27.12.2025 - 10.01.2026
При оплате криптовалютой:
Ваша прибыль 466.19 RUB / 5.25 USDT
- Наявність: В наявності
- Виробник: OmniVision AG
- Модель: 3023088
- ATC-код S01BA01
- EAN 7680310690257
Склад:
Опис
Was ist Spersadex mono 0,1% Augentropfen und wann wird es angewendet?
Spersadex mono 0,1% Augentropfen enthalten eine entzündungshemmende Substanz (das Kortikosteroid Dexamethason). Sie werden bei nicht-infektiösen Entzündungen im vorderen Augenabschnitt (besonders wenn diese allergischen Ursprungs sind) angewendet.
Spersadex mono 0,1% darf nur auf Verschreibung des Arztes, bzw. der Ärztin angewendet werden.
Was sollte dazu beachtet werden?
- Das Arzneimittel nie von sich aus zur Behandlung anderer Erkrankungen oder für Drittpersonen verwenden.
- Während der gesamten Behandlungsdauer mit diesem Arzneimittel sind regelmässige Kontrollen Ihrer Augen durch den Arzt bzw. die Ärztin erforderlich.
Wann dürfen Spersadex mono 0,1% Augentropfen nicht angewendet werden?
- Wenn Sie auf den Wirkstoff Dexamethason, oder andere Inhaltsstoffe von Spersadex mono 0,1% Augentropfen allergisch sind.
- Wenn Erkrankungen wie grüner Star (Glaukom), Geschwüre oder äussere Verletzungen der Hornhaut vorhanden sind.
- Bei Augenerkrankungen, welche durch Viren, Bakterien oder Pilze verursacht wurden.
Wann ist bei der Anwendung von Spersadex mono 0,1% Augentropfen Vorsicht geboten?
Dieses Arzneimittel kann Nebenwirkungen haben, welche das Sehvermögen beeinträchtigen können (siehe «Welche Nebenwirkungen kann Spersadex mono 0,1% Augentropfen haben?»). Nehmen Sie nicht am Strassenverkehr teil und bedienen Sie keine Maschinen, bis diese Beeinträchtigungen abgeklungen sind.
Kortikosteroide können eine Infektion am Auge maskieren, aktivieren oder verschlimmern. Wird Spersadex mono 0,1% während längerer Zeit angewendet, kann dies zu verzögerter Wundheilung führen. Ebenso kann es zu Erhöhung des Augeninnendruckes und als Folge zu einem Glaukom kommen. Während der Behandlung mit Spersadex mono 0,1% sollten Sie unter ständiger medizinischer Kontrolle stehen, wobei der Augeninnendruck regelmässig vom Arzt bzw. von der Ärztin zu messen ist. Dies ist besonders bei Kindern und Jugendlichen wichtig, da ein durch Spersadex mono 0,1% ausgelöster erhöhter Augeninnendruck schneller auftreten kann als bei Erwachsenen.
Wenn sich die mit Spersadex mono 0,1% behandelten Augenbeschwerden nach 2-3 Behandlungstagen verschlechtern oder wenn neue Symptome auftreten, sollten Sie unverzüglich Ihren Arzt bzw. Ihre Ärztin konsultieren.
Wenn Sie unter Krankheiten leiden, welche ein dünner werden von Geweben am Auge (Hornhaut oder Sklera) zur Folge haben: Lokale Anwendung von Kortikosteroiden kann eine Perforation des Auges verursachen.
Bei Vorliegen von Diabetes (insbesondere Typ I Diabetes) besteht das Risiko eines Kataraktes. Bei Anwendung von Kortikosteroiden bei Diabetikern erhöht sich die Gefahr eines frühen und schnell auftretenden Kataraktes.
Wenn eine Schwellung am Rumpf und im Gesicht auftritt (Cushing Syndrom), sollten Sie Ihren Arzt informieren.
Die gleichzeitige Anwendung von Spersadex mono 0,1% und Mydriatika erhöht das Risiko einer Augeninnendrucksteigerung. Wird Spersadex mono 0,1% mit Antiglaukom-Medikationen kombiniert, so können die Wirkungen der verabreichten Präparate beeinträchtigt werden.
Da der Wirkstoff von Spersadex mono 0,1% auch nach lokaler Applikation in die Blutbahn gelangen kann, ist bei der Anwendung bei Patienten mit Blutdruckproblemen besondere Vorsicht geboten.
Informieren Sie Ihren Arzt bzw. Ihre Ärztin, wenn Sie an anderen Krankheiten leiden (wie beispielsweise erhöhter Augeninnendruck, Herz-Kreislauferkrankungen, Bluthochdruck, Herzrhythmusstörungen oder Alters-Zuckerkrankheit, Schilddrüsenüberfunktion, «trockene Nasenschleimhaut») oder wenn Sie Allergien haben.
Die Anwendung von Spersadex mono 0,1% Augentropfen bei Kindern unter 2 Jahren wird nicht empfohlen.
Da Spersadex mono 0,1% Augentropfen nicht mit jedem anderen Arzneimittel (auch Tabletten mit bestimmten Wirkstoffen) kombiniert werden kann, sollten Sie, falls Sie gleichzeitig mit Spersadex mono 0,1% Augentropfen noch andere Arzneimittel (auch selbstgekaufte) einnehmen oder am Auge anwenden, dies mit dem Arzt bzw. der Ärztin besprechen, damit ein optimaler Zeitplan für die einzelnen Anwendungen aufgestellt werden kann. Zwischen zwei lokal am Auge verabreichten Arzneimitteln muss ein Abstand von 5 Minuten zwischen den einzelnen Anwendungen eingehalten werden.
Um langwierige Komplikationen zu vermeiden, die durch Anwendung eines falsch gewählten oder falsch dosierten Augenpräparates hervorgerufen werden können, dürfen Sie Spersadex mono 0,1% (auch bei späteren neuen Entzündungen) nicht ohne ärztliche Verordnung anwenden.
Sofern nach 7-8 Behandlungstagen keine Besserung Ihrer Augenerkrankung erreicht wird, müssen Sie unbedingt Ihren Augenarzt bzw. Ihre Augenärztin konsultieren.
Hinweis für Kontaktlinsenträger
Spersadex mono 0,1% enthält Benzalkonium, ein Konservierungsmittel, das Augenirritationen hervorrufen kann und weiche Kontaktlinsen verfärbt. Kontakt mit weichen Linsen ist zu vermeiden. Nach der Behandlung mit Spersadex mono 0,1% müssen Sie mindestens 15 Minuten warten, bis die Linsen wieder eingesetzt werden können.
Dürfen Spersadex mono 0,1% Augentropfen während einer Schwangerschaft oder in der Stillzeit angewendet werden?
Die Anwendung während der Schwangerschaft wird nicht empfohlen.
Die Anwendung in der Stillzeit darf nur mit ausdrücklicher Genehmigung Ihres Arztes bzw. Ihrer Ärztin erfolgen.
Wie verwenden Sie Spersadex mono 0,1% Augentropfen?
Erwachsene, Jugendliche und Kinder ab 2 Jahren
Pro Tag werden 3-5 mal 1 Tropfen in den Bindehautsack des betroffenen Auges gegeben. Mit einer Hand das Tropffläschchen bei nach hinten geneigtem Kopf möglichst senkrecht über das Auge halten, mit der anderen Hand das Unterlid leicht nach unten ziehen und durch Druck auf das Fläschchen einen Tropfen in den Bindehautsack fallen lassen (vermeiden Sie eine Berührung des Auges oder des Unterlids mit dem Tropfansatz). Aus Sterilitätsgründen auch darauf achten, dass während der Anwendung der Flaschenhals und die Tropferspitze weder mit den Händen noch mit Gegenständen in Berührung kommt.
Die Anwendung von Spersadex mono 0,1% bei Kindern unter 2 Jahren wird nicht empfohlen.
Wenn zuviel Spersadex mono 0,1% ins Auge gelangt ist, spülen Sie das Auge mit lauwarmem Wasser aus. Tropfen Sie nicht mehr nach, bis es Zeit für die nächste planmässige Anwendung ist.
Wenn Sie einmal vergessen haben, Spersadex mono 0,1% einzutropfen setzen Sie die Behandlung planmässig fort. Tropfen Sie nicht die doppelte Dosis ein, um die versäumte Dosis nachzuholen.
Ändern Sie nicht von sich aus die vom Arzt bzw. von der Ärztin verschriebene Dosierung. Weder die tägliche Dosis noch die Therapiedauer dürfen ohne Rücksprache mit Ihrem Arzt bzw. Ihrer Ärztin geändert werden. In akuten Fällen wird Sie der Arzt bzw. die Ärztin über eine häufigere Anwendung informieren. Wenn Sie glauben, das Arzneimittel wirke zu schwach oder zu stark, so sprechen Sie mit Ihrem Arzt oder Apotheker bzw. Ihrer Ärztin oder Apothekerin.
Welche Nebenwirkungen kann Spersadex mono 0,1% Augentropfen haben?
Folgende Nebenwirkungen können nach der Anwendung von Spersadex mono 0,1% auftreten:
Häufig (kann bis zu 10 von 100 behandelten Personen betreffen):
Auswirkungen auf die Augen: Unbehagen.
Gelegentlich (kann bis zu 1 von 100 behandelte Personen betreffen):
Auswirkungen auf die Augen: Hornhautentzündung, trockene Augen, Bindehautentzündung, Lichtempfindlichkeit, verschwommene Sicht, Juckreiz, Fremdkörpergefühl, verstärkter Tränenfluss, anormale Sinnesempfindungen im Auge, Lidrandverkrustungen, Irritationen, Rötung.
Auswirkungen auf den Körper: Geschmacksstörungen.
Die Erfahrungen nach Markteinführung zeigen die folgenden Nebenwirkungen:
Überempfindlichkeitsreaktionen (Allergien), Benommenheit, Kopfschmerzen, Schwellung am Rumpf und Gesicht (Cushing Syndrom), Nebennierenunterfunktion, Hornhautentzündung, erhöhter Augendruck, Grüner Star (Glaukom), verminderte Sehschärfe, Herabhängen des Augenlides, Hornhauterrosion, Augenschmerzen, erweiterte Pupillen.
In sehr seltenen Fällen entwickelten Patienten mit ausgeprägten Hornhautschädigungen unter Behandlung mit phosphathaltigen Augentropfen Trübungen der Hornhaut durch Kalkablagerungen.
Wenn Sie Nebenwirkungen bemerken, die hier nicht beschrieben sind, sollten Sie Ihren Arzt oder Apotheker bzw. Ihre Ärztin oder Apothekerin informieren.
In den Augenpräparaten enthaltene Wirkstoffe können in den Blutkreislauf gelangen. Nebenwirkungen können deshalb ausser am Auge auch an anderen Stellen des Körpers auftreten.
Was ist ferner zu beachten?
Das Arzneimittel darf nur bis zu dem auf dem Behälter mit «EXP» bezeichneten Datum verwendet werden.
Flasche nach Gebrauch sofort verschliessen. Bewahren Sie Spersadex mono 0,1% in der verschlossenen Originalpackung bei Raumtemperatur (15-25 °C) auf.
Nach Anbruch der Flasche Spersadex mono 0,1% nicht länger als einen Monat verwenden.
Nach Beendigung der Behandlung das Arzneimittel mit dem restlichen Inhalt Ihrem Arzt oder Apotheker bzw. Ihrer Ärztin oder Apothekerin zum Vernichten bringen.
Arzneimittel sollten Sie grundsätzlich für Kinder unerreichbar aufbewahren.
Weitere Auskünfte erteilt Ihnen Ihr Arzt oder Apotheker, bzw. Ihre Ärztin oder Apothekerin. Diese Personen verfügen über die ausführliche Fachinformation.
Was ist in Spersadex mono 0,1% Augentropfen enthalten?
1 ml Spersadex mono 0,1% enthält als Wirkstoff 1 mg Dexamethason-Natriumphosphat, als Konservierungsmittel Benzalkoniumchlorid und weitere Hilfsstoffe.
Zulassungsnummer
31069 (Swissmedic).
Wo erhalten Sie Spersadex mono 0,1% Augentropfen? Welche Packungen sind erhältlich?
In Apotheken gegen ärztliche Verschreibung, die nur zum einmaligen Bezug berechtigt.
Tropfflasche zu 5 ml Augentropfen.
Zulassungsinhaberin
OmniVision AG, 8212 Neuhausen.
Diese Packungsbeilage wurde im Oktober 2018 letztmals durch die Arzneimittelbehörde (Swissmedic) geprüft.
Qu’est-ce que Spersadex mono 0,1% et quand doit-il être utilisé?
Le collyre Spersadex mono 0,1% contient une substance anti-inflammatoire (le corticostéroïde dexaméthasone). Il est utilisé en cas d'inflammations non infectieuses de la partie antérieure de l'œil (surtout lorsqu'elles sont d'origine allergique).
Spersadex mono 0,1% ne doit être utilisé que sur prescription du médecin.
De quoi faut-il tenir compte en dehors du traitement?
- N'utilisez jamais ce médicament de votre propre chef pour le traitement d'une autre maladie que celle dont vous souffrez ou pour d'autres personnes.
- Il est indispensable que le médecin contrôle régulièrement vos yeux tant que vous utilisez ce médicament.
Quand Spersadex mono 0,1% ne doit-il pas être utilisé?
- En cas d'allergie au principe actif dexaméthasone ou à d'autres substances contenues dans le collyre Spersadex mono 0,1%.
- Lors d'affections telles que glaucome, ulcères ou lésions externes de la cornée.
- En cas de lésions oculaires provoquées par des virus, des bactéries ou par des champignons.
Quelles sont les précautions à observer lors de l’utilisation de Spersadex mono 0,1%?
Les effets indésirables de ce médicament peuvent entraver l'acuité visuelle (voir «Quels effets secondaires Spersadex mono 0,1% peut-il provoquer?»). Ne participez pas activement au trafic routier et n'utilisez pas de machines jusqu'à ce que cette entrave ait disparu.
Les corticostéroïdes peuvent masquer, activer ou aggraver une infection de l'œil. L'application de Spersadex mono 0,1% pendant une période de temps prolongée peut conduire à un retard de cicatrisation. De même, son utilisation peut conduire à une augmentation de la pression intraoculaire et par conséquent à un glaucome. Pendant le traitement par Spersadex mono 0,1%, vous devez rester sous contrôle médical permanent, pour que le médecin puisse mesurer régulièrement votre pression intraoculaire. Cela est particulièrement important pour les enfants et les adolescents, chez qui une augmentation de la pression intraoculaire causée par Spersadex mono 0,1% peut apparaître plus rapidement que chez les adultes.
Si les troubles oculaires traités s'aggravent après 2 ou 3 jours de traitement ou si vous observez de nouveaux symptômes, consultez immédiatement votre médecin.
Si vous souffrez de maladies qui amincissent les tissus de l'œil (cornée ou sclérotique): l'application locale de corticostéroïdes peut provoquer une perforation de l'œil.
Le diabète (surtout de type I) s'accompagne d'un risque de cataracte. L'utilisation de corticostéroïdes chez des diabétiques augmente le risque de survenue précoce et rapide d'une cataracte.
Si un gonflement du tronc ou du visage apparaît (syndrome de Cushing), informez-en votre médecin. L'utilisation concomitante de mydriatique et de Spersadex mono 0,1% augmente le risque d'élévation de la pression intraoculaire. L'association de Spersadex mono 0,1% à des médicaments contre le glaucome peut altérer les effets des médicaments administrés.
Parce que le principe actif de Spersadex mono 0,1% peut parvenir dans la circulation sanguine même après application locale, une prudence particulière est recommandée chez les patients souffrant de problèmes de tension.
Veuillez informer votre médecin ou votre pharmacien si vous souffrez d'une autre maladie (comme par exemple une élévation de la pression intraoculaire, une maladie cardio-vasculaire, une hypertension artérielle, des troubles du rythme cardiaque ou un diabète sucré lié à l'âge, une hyperfonction des glandes thyroïdiennes, une «sécheresse de la muqueuse nasale») ou si vous êtes allergique.
L'utilisation du collyre Spersadex mono 0,1% chez les enfants âgés moins de 2 ans n'est pas recommandée.
Le collyre Spersadex mono 0,1% ne peut pas être associé avec n'importe quel autre médicament (y compris des comprimés avec certains principes actifs). C'est pourquoi, si vous prenez déjà d'autres médicaments en usage interne ou en application dans l'œil (même en automédication) en même temps que Spersadex mono 0,1%, vous devez en informer votre médecin, afin de prévoir un horaire optimal pour les différentes applications.
Si deux médicaments doivent être appliqués localement dans l'œil, il faudra attendre 5 minutes entre les différentes instillations. Pour éviter les complications fastidieuses dues à l'utilisation d'un produit oculaire mal choisi ou mal dosé, Spersadex mono 0,1% ne doit pas être utilisé sans prescription médicale (également lors de nouvelles inflammations ultérieures).
Si aucune amélioration de vos troubles oculaires ne se manifeste après 7 ou 8 jours de traitement, veuillez immédiatement consulter votre ophtalmologue.
Remarque pour les porteurs de lentilles de contact
Spersadex mono 0,1% contient du benzalkonium, un agent conservateur qui peut causer des irritations aux yeux et qui décolore les lentilles de contact souples. Éviter le contact avec les lentilles souples. Après l'application de Spersadex mono 0,1%, vous devez attendre au moins 15 minutes avant de remettre vos lentilles.
Spersadex mono 0,1% peut-il être utilisé pendant la grossesse ou l’allaitement?
L'utilisation pendant la grossesse est déconseillée.
Pendant l'allaitement, n'utilisez ce médicament qu'avec l'autorisation expresse de votre médecin.
Comment utiliser Spersadex mono 0,1%?
Adultes, adolescents et enfants à partir de 2 ans
Instiller 1 goutte 3 à 5×/jour dans le sac conjonctival de l'œil atteint. Pencher la tête en arrière et tenir d'une main le flacon compte-gouttes le plus verticalement possible au-dessus de l'œil. Tirer la paupière inférieure légèrement vers le bas avec l'autre main et laisser tomber une goutte dans le sac conjonctival en appuyant sur le flacon (éviter de toucher l'œil ou la paupière inférieure avec l'embout du flacon). Pour des raisons de stérilité, veillez également à ce que ni le goulot ni l'embout du flacon n'entrent en contact avec les mains ou avec d'autres objets.
L'utilisation de Spersadex mono 0,1% chez les enfants âgés moins de 2 ans n'est pas recommandée.
Si vous avez mis trop de Spersadex mono 0,1% dans un œil, rincez-le à l'eau tiède. Ne remettez pas de gouttes jusqu'au moment prévu de la dose suivante.
Si vous avez oublié une dose de Spersadex mono 0,1%, poursuivez le traitement de la manière prescrite. Ne mettez pas deux fois plus de gouttes pour compenser la dose manquée.
Ne changez pas de votre propre chef le dosage prescrit. Ni la dose quotidienne, ni la durée du traitement ne doivent être modifiées sans avis médical. Pour les cas aigus, le médecin décidera d'une application plus fréquente. Adressez-vous à votre médecin ou à votre pharmacien si vous estimez que l'efficacité du médicament est trop faible ou au contraire trop forte.
Quels effets secondaires Spersadex mono 0,1% peut-il provoquer?
L'utilisation de Spersadex mono 0,1% peut provoquer les effets secondaires suivants:
Fréquents (jusqu'à 10 personnes sur 100):
Effets sur les yeux: inconfort.
Occasionnels (jusqu'à 1 personne sur 100):
Effets sur les yeux: inflammation de la cornée, sécheresse oculaire, conjonctivite, sensibilité à la lumière, vision trouble, démangeaisons, sensation de corps étranger, augmentation du larmoiement, sensations anormales dans l'œil, formation de croûtes sur le bord de la paupière, irritations, rougeurs.
Effets sur l'organisme: altération du goût.
L'expérience après la commercialisation a montré les effets secondaires suivants:
Réactions d'hypersensibilité (allergies), sensations de vertiges, maux de tête, gonflement du tronc et du visage (syndrome de Cushing), insuffisance surrénalienne, inflammation de la cornée, augmentation de la pression intraoculaire, glaucome, acuité visuelle diminuée, descente de la paupière, érosion de la cornée, douleur oculaire, agrandissement des pupilles.
Dans de très rares cas, des patients présentant des défauts cornéens prononcés ont développé sous traitement par des collyres contenant des phosphates des opacités de la cornée due à la calcification.
Si vous remarquez d'autres effets secondaires, veuillez en informer votre médecin ou votre pharmacien.
Les principes actifs contenus dans les produits oculaires peuvent parvenir dans la circulation sanguine. Par conséquent, les effets secondaires ne se limitent pas seulement à l'œil, mais peuvent également apparaître à d'autres endroits du corps.
À quoi faut-il encore faire attention?
Le médicament ne doit pas être utilisé au-delà de la date figurant après la mention «EXP» sur le récipient.
Refermer le flacon immédiatement après emploi. Conserver Spersadex mono 0,1% dans l'emballage d'origine fermé à température ambiante (15–25 °C). Une fois entamé, le flacon de Spersadex mono 0,1% ne doit pas être utilisé pendant plus de 1 mois.
Une fois le traitement terminé, veuillez rapporter le reste du médicament à votre médecin ou pharmacien pour l'élimination.
Les médicaments doivent être conservés hors de portée des enfants.
Pour de plus amples renseignements, consultez votre médecin ou votre pharmacien, qui disposent d'une information détaillée destinée aux professionnels.
Que contient Spersadex mono 0,1%?
1 ml de Spersadex mono 0,1% contient comme principe actif 1 mg de déxamethasone-phosphate de sodium, comme conservateur le chlorure de benzalkonium et d'autres excipients.
Numéro d’autorisation
31069 (Swissmedic).
Où obtenez-vous Spersadex mono 0,1%? Quels sont les emballages à disposition sur le marché?
En pharmacie, seulement sur ordonnance médicale non renouvelable.
Flacon compte-gouttes de 5 ml de collyre.
Titulaire de l’autorisation
OmniVision AG, 8212 Neuhausen.
Cette notice d'emballage a été vérifiée pour la dernière fois en octobre 2018 par l'autorité de contrôle des médicaments (Swissmedic).
Che cos’è Spersadex mono 0,1% e quando si usa?
Le gocce oftalmiche Spersadex mono 0,1% contengono una sostanza antiflogistica (il corticosteroide desametasone) e viene impiegato in caso di infiammazioni non infettive della parti anteriori dell'occhio (soprattutto se sono di natura allergica).
Spersadex mono 0,1% può solo essere usato su prescrizione medica.
Di che cosa occorre inoltre tener conto durante il trattamento?
- Non utilizzare il medicamento di propria iniziativa per il trattamento di altre malattie o su altre persone.
- Durante tutta la durata del trattamento con questo medicamento sono necessari periodici controlli dei suoi occhi da parte del medico.
Quando non si può usare Spersadex mono 0,1%?
- In caso d'ipersensibilità al principio attivo desametasone o un altro componente delle gocce oftalmiche Spersadex mono 0,1%.
- Nel caso sia affetto(-a) da glaucoma, presenti ulcere o ferite esterne della cornea.
- Nel caso di malattie oculari causate da virus, batteri o funghi.
Quando è richiesta prudenza nell’uso di Spersadex mono 0,1%?
Gli effetti collaterali di questo medicamento possono alterare l'acuità visiva (vedi «Quali effetti collaterali può avere Spersadex mono 0,1%?»). Non prenda parte attiva al traffico e non manovra macchine finché questi peggioramenti scompaiono.
I corticosteroidi possono mascherare, attivare o aggravare le infezioni dell'occhio. L'assunzione di Spersadex mono 0,1% per un periodo di tempo più lungo può portare a un ritardo nella cicatrizzazione delle ferite. Altrettanto, può aumentare la pressione intraoculare e, di conseguenza, causare un glaucoma. Durante il trattamento con Spersadex mono 0,1% dovrà essere sotto costante controllo del medico, il quale dovrà misurarle regolarmente la pressione intraoculare. Ciò è particolarmente importante nei bambini e negli adolescenti, nei quali Spersadex mono 0,1% può causare un aumento della pressione intraoculare più rapidamente che negli adulti.
Consulti immediatamente il suo medico se dopo 2-3 giorni i disturbi derivanti dal trattamento con Spersadex mono 0,1% peggiorano o se si manifestano nuovi sintomi.
Se soffre di malattie che causano un assottigliamento dei tessuti dell'occhio (della cornea o della sclera), l'applicazione locale di corticosteroidi può causare una perforazione dell'occhio.
In caso di diabete (soprattutto con diabete di tipo I) sussiste il rischio di cataratta. L'utilizzo di corticosteroidi da parte dei diabetici aumenta il rischio di una cataratta precoce e rapida.
Informi il medico se manifesta gonfiore a livello del tronco e in viso (sindrome di Cushing). L'uso concomitante di midriatica e Spersadex mono 0,1% aumenta il rischio di ipertensione intraoculare. Se Spersadex mono 0,1% viene combinato con medicamenti anti-glaucoma, gli effetti dei farmaci somministrati possono essere compromessi.
Dato che il principio attivo di Spersadex mono 0,1% può entrare nella circolazione sanguinea anche dopo un'applicazione locale, è necessario usare particolare prudenza in pazienti con disturbi della pressione arteriosa.
Informi il suo medico nel caso in cui soffre di altre malattie (come per esempio aumento della pressione intraoculare, malattie cardiocircolatorie, ipertensione arteriosa, aritmia o diabete anziano, ipertiroidisma, «mucosa nasale secca») o se soffre di allergie.
L'uso delle gocce oftalmiche Spersadex mono 0,1% nei bambini al di sotto dei 2 anni non è raccomandato.
Le gocce oftalmiche Spersadex mono 0,1% non possono essere combinate con qualsiasi altro medicamento (anche compresse con definiti principi attivi). Perciò, se contemporaneamente all'uso di Spersadex mono 0,1%, assume o applica agli occhi altri medicamenti (anche se acquistati di sua iniziativa), dovrebbe informare il medico curante per impostare un programma ottimale per le singole applicazioni. Un intervallo di 5 minuti dev'essere osservato tra due medicamenti somministrati localmente negli occhi.
Per evitare lunghe complicazioni che possono essere causate dall'applicazione di un farmaco per gli occhi scelto in modo inappropriato oppure in dosi sbagliate, non deve usare Spersadex mono 0,1% (nemmeno in caso di nuove infiammazioni ulteriori) senza aver consultato il medico.
Se, dopo 7-8 giorni di cura, i disturbi agli occhi non migliorano, informi assolutamente il suo oculista.
Portatori di lenti a contatto
Spersadex mono 0,1% contiene il benzalconio, un conservante che può provocare irritazioni agli occhi e scolorire le lenti a contatto morbide. Si consiglia pertanto di evitare il contatto con le lenti morbide. Successivamente al trattamento con Spersadex mono 0,1%, deve attendere almeno 15 minuti prima di applicare nuovamente le lenti a contatto.
Si può usare Spersadex mono 0,1% durante la gravidanza o l’allattamento?
L'uso durante la gravidanza non è raccomandato.
Durante l'allattamento, il medicamento può essere utilizzato solo con l'esplicita autorizzazione del medico.
Come usare Spersadex mono 0,1%?
Adulti, adolescenti e bambini a partire dai 2 anni
Applicare, 3-5 volte al giorno, 1 goccia nel sacco congiuntivale dell'occhio affetto. Tenere il flacone con una mano il più verticalmente possibile sopra l'occhio, a testa inclinata all'indietro, con l'altra mano tirare leggermente verso il basso la palpebra inferiore, lasciando cadere la goccia nel sacco congiuntivale con una leggera pressione sul flacone (evitare il contatto fra l'occhio o la palpebra e la punta del flacone). Per motivi di sterilità bisogna evitare il contatto tra la punta del flacone e le mani o altri oggetti.
L'uso di Spersadex mono 0,1% è sconsigliato nei bambini al di sotto dei 2 anni.
Se viene instillata una dose eccessiva di Spersadex mono 0,1% nell'occhio, lavi subito con acqua tiepida. Non usi il collirio fino all'applicazione programmata successiva.
Se ha dimenticato una volta di instillare Spersadex mono 0,1%, prosegua il trattamento come stabilito. Non instilli una dose doppia per compensare eventuali dimenticanze.
Non modifichi di propria iniziativa la posologia prescritta. Né la dose giornaliera né la durata della terapia devono venire modificate senza aver consultato il medico. In casi acuti il medico lei fornirà informazioni per un impiego più frequente. Se ritiene che l'azione del medicamento sia troppo debole o troppo forte ne parli al suo medico o al suo farmacista.
Quali effetti collaterali può avere Spersadex mono 0,1%?
In seguito all'applicazione di Spersadex mono 0,1% possono manifestarsi i seguenti effetti collaterali:
Frequenti (fino a 10 persone su 100):
Effetti sull'occhio: fastidio.
Occasionali (fino a 1 persona su 100):
Effetti sull'occhio: infiammazione della cornea, occhi secchi, congiuntivite, sensibilità alla luce, visione offuscata, prurito, sensazione di corpo estraneo, lacrimazione aumentata, sensazioni anomale nell'occhio, formazione di croste sulla palpebra, irritazione, arrossamento.
Effetti sul corpo: patologie del gusto.
Nel periodo successivo alla commercializzazione sono stati osservati i seguenti effetti collaterali:
Reazioni di ipersensibilità (allergie), vertigini, mal di testa, gonfiore del tronco e in viso (sindrome di Cushing), ipofunzione surrenalica, infiammazione della cornea, aumento della pressione oculare, glaucoma, acutezza visiva ridotta, penzolare della palpebra, erosione corneale, dolore oculare, pupille dilatate.
In casi molto rari, i pazienti affetti da gravi difetti della cornea in terapia con colliri contenenti fosfato sviluppano opacità corneali a causa della calcificazione.
Se osserva effetti collaterali qui non descritti, dovrebbe informare il suo medico o il suo farmacista.
Le sostanze attive contenute nei preparati oftalmiche possono entrare nella circolazione del sangue. Perciò degli effetti collaterali, oltre che dell'occhio, possono manifestarsi anche in altre parti del corpo.
Di che altro occorre tener conto?
Il medicamento non dev'essere utilizzato oltre la data indicata con «EXP» sulla confezione.
Chiudere il flacone subito dopo l'uso. Conservi le gocce oftalmiche Spersadex mono 0,1% nella confezione originale a temperatura ambiente (15-25 °C). Dopo aver aperto per la prima volta il flacone di Spersadex mono 0,1%, il contenuto non può essere usato più a lungo di 1 mese.
A cura terminata, porti il resto del medicamento al medico o al farmacista per l'eliminazione.
I farmaci vanno conservati, per principio, al di fuori della portata dei bambini.
Il medico o il farmacista, che sono in possesso di documentazione professionale dettagliata, possono darle ulteriori informazioni.
Cosa contiene Spersadex mono 0,1%?
1 ml di Spersadex mono 0,1% contiene come principio attivo 1 mg di desametasone-sodiofosfato, come conservante il benzalconio cloruro ed altre sostanze ausiliarie.
Numero dell’omologazione
31069 (Swissmedic).
Dove è ottenibile Spersadex mono 0,1%? Quali confezioni sono disponibili?
In farmacia dietro presentazione della prescrizione medica non rinnovabile.
Flacone contagocce da 5 ml di gocce oftalmiche.
Titolare dell’omologazione
OmniVision AG, 8212 Neuhausen.
Questo foglietto illustrativo è stato controllato l'ultima volta nell'ottobre 2018 dall'autorità competente in materia di medicamenti (Swissmedic).
Zusammensetzung
Wirkstoff: Dexamethasoni natrii phosphas.
Hilfsstoffe: Conserv.: Benzalkonii chloridum, Excipiens ad solutionem.
Galenische Form und Wirkstoffmenge pro Einheit
Augentropfen: Dexamethasoni natrii phosphas 1 mg/ml.
Indikationen/Anwendungsmöglichkeiten
Nicht infektiöse Konjunktivitiden, Keratitiden und Blepharitiden, insbesondere allergischer Genese, Entzündungen der vorderen Uvea (Iritis, Iridocyclitis), Skleritis, Episkleritis und orbitale Myositis. Sympathische Ophthalmie.
Dosierung/Anwendung
Erwachsene, Jugendliche und Kinder ab 2 Jahren
3-5 mal täglich 1 Tropfen in den Bindehautsack applizieren.
Akute Fälle: bis 1 Tropfen stündlich. Sofern nach 7-8 Behandlungstagen keine Besserung erreicht wird, sind andere therapeutische Massnahmen zu erwägen.
Kinder unter 2 Jahren
Wegen der Gefahr systemischer Glukokortikoid-Wirkungen wird von der Anwendung bei Kindern unter 2 Jahren abgeraten.
Kontraindikationen
- Überempfindlichkeit gegenüber dem Wirkstoff oder einem der Hilfsstoffe.
- Verletzungen und ulzeröse Prozesse der Hornhaut.
- Herpes simplex (Keratitis dendritica), Vaccinia, Varicella und alle anderen Viruserkrankungen der Kornea und der Konjunktiva.
- Mykobakterielle Augeninfektionen.
- Mykosen des Augengewebes oder unbehandelte parasitäre Augeninfektionen.
- Bakterielle Augeninfektionen.
- Glaukom.
- Steroide sollten generell nach unkomplizierter Entfernung eines Fremdkörpers aus der Kornea nicht angewendet werden.
- Spersadex mono 0,1% sollte Neugeborenen ebenfalls nicht verabreicht werden.
Warnhinweise und Vorsichtsmassnahmen
Allgemeine Vorsichtsmassnahmen
Kortikosteroide können Resistenzen gegen bakterielle, virale, mykotische oder parasitäre Infektionen verringern sowie deren Etablierung begünstigen und die klinischen Anzeichen einer Infektion maskieren.
Bei Ulzeration der Kornea muss eine Pilzinfektion in Betracht gezogen werden. Bei Auftreten einer Pilzinfektion muss die Kortikosteroidbehandlung abgebrochen werden.
Wird Spersadex mono 0,1% während längerer Zeit angewendet, kann dies zu verzögerter Wundheilung führen. Eine gleichzeitige Behandlung mit nichtsteroidalen Entzündungshemmern (NSAIDs) oder eine systemische Behandlung mit Kortikosteroiden verzögern die Wundheilung ebenfalls (siehe «Interaktionen»).
Bei Krankheiten, die ein Dünnerwerden der Kornea oder Sklera zur Folge haben, kann die Anwendung von Steroiden Perforationen hervorrufen.
Ebenso kann es zur Erhöhung des intraokulären Druckes und als Folge zu einem Glaukom, zu Schäden am Sehnerv, reduzierter Sehschärfe und Sehschwäche kommen. Während der Behandlung mit Spersadex mono 0,1% sollen die Patienten unter ständiger medizinischer Kontrolle stehen, wobei der intraokuläre Druck regelmässig vom Arzt zu messen ist. Dies ist vor allem bei Kindern und Jugendlichen wichtig, da eine kortikosteroidinduzierte okuläre Hypertonie schneller auftreten kann als bei Erwachsenen.
Nach intensiver oder längerer kontinuierlicher Anwendung kann, in Zusammenhang mit systemischer Resorption von okulär verabreichtem Dexamethason, bei prädisponierten Patienten, einschliesslich Kinder und mit Ritonavir behandelten Patienten (siehe «Interaktionen») ein Cushing-Syndrom und/oder eine Nebennierensuppression auftreten. In diesen Fällen sollte die Behandlung nicht abrupt abgebrochen werden, sondern stufenweise ausschleichend.
Auch andere systemische Glukokortikoidwirkungen können bei langer Therapiedauer mit hohen Dosen nicht ausgeschlossen werden.
Durch die erhöhte Permeabilität der Linse kann es zu einem subkapsulären posterioren Katarakt kommen. Bei prädisponierten Patienten, z.B. Diabetes, insbesondere Typ I Diabetes, ist die Gefahr einer Kataraktbildung erhöht.
Die Verschreibung von Spersadex mono 0,1% sollte in jedem Fall nur nach gründlicher augenärztlicher Kontrolle erfolgen.
Hinweis für Kontaktlinsenträger
Es wird davon abgeraten, während der Behandlung einer Augenentzündung Kontaktlinsen zu tragen. Spersadex mono 0,1% enthält Benzalkoniumchlorid, das Augenreizungen verursachen kann und bei weichen Kontaktlinsen bekanntermassen zu Verfärbungen führt. Vermeiden Sie den Kontakt mit weichen Kontaktlinsen. Wenn der Arzt jedoch die Verwendung von Kontaktlinsen als angemessen erachtet, muss der Patient angewiesen werden, die Kontaktlinsen vor der Verabreichung von Spersadex mono 0,1% zu entfernen und mindestens 15 Minuten bis zum Wiedereinsetzen zu warten.
Kinder und Jugendliche
Wegen der Gefahr von systemischen Reaktionen wird von der Verwendung bei Kindern unter 2 Jahren abgeraten.
Interaktionen
Die gleichzeitige Anwendung von Spersadex mono 0,1% und Mydriatika erhöht das Risiko einer Steigerung des intraokulären Drucks.
Wird Spersadex mono 0,1% mit Antiglaukom-Medikationen kombiniert, so können die Wirkungen der verabreichten Präparate beeinträchtigt werden.
Die gleichzeitige Anwendung von topischen Steroiden und topischen NSAR kann das Risiko für Probleme hinsichtlich der Hornhautheilung erhöhen (siehe «Warnhinweise und Vorsichtsmassnahmen»).
Bei mit Ritonavir behandelten Patienten sind die Plasmakonzentrationen von Dexamethason gegebenenfalls erhöht (siehe «Warnhinweise und Vorsichtsmassnahmen»).
Schwangerschaft/Stillzeit
Schwangerschaft
Es existieren keine adäquaten oder gut kontrollierten Studien zur Beurteilung von Spersadex mono 0,1% bei schwangeren Frauen. Die längere oder wiederholte Verwendung von Kortikoiden wurde mit einem erhöhten Risiko für intrauterine Wachstumsretardierung in Verbindung gebracht. Kinder, die von Müttern geboren wurden, die während der Schwangerschaft erhebliche Dosen von Kortikosteroiden erhalten haben, sollten sorgfältig hinsichtlich Anzeichen von Nebennierenschwäche beobachtet werden (siehe «Warnhinweise und Vorsichtsmassnahmen»). Studien an Tieren haben eine Reproduktionstoxizität nach der systemischen Verabreichung ergeben. Die okulare Verabreichung von 0,1% Dexamethason resultierte zudem in fetalen Anomalien bei Kaninchen (siehe «Präklinische Daten»).
Spersadex mono 0,1% wird während der Schwangerschaft nicht empfohlen.
Stillzeit
Es ist nicht bekannt, ob Spersadex mono 0,1% in der menschlichen Muttermilch ausgeschieden wird. Zur Ausscheidung von Dexamethason in der menschlichen Muttermilch sind keine Daten verfügbar. Es ist unwahrscheinlich, dass, infolge der Verwendung des Produkts durch die Mutter, die Menge an Dexamethason in der menschlichen Muttermilch nachweisbar wäre oder in der Lage wäre, klinische Auswirkungen auf das Kind zu haben.
Es kann nicht ausgeschlossen werden, dass ein Risiko für das gesäugte Kind besteht. Es muss, unter Berücksichtigung der Vorteile des Stillens für das Kind und der Vorteile der Therapie für die Frau, entschieden werden, ob das Stillen eingestellt oder die Therapie abgebrochen/unterlassen wird.
Wirkung auf die Fahrtüchtigkeit und auf das Bedienen von Maschinen
Vorübergehendes Verschwommensehen und andere Seheinschränkungen können die Fähigkeit beeinträchtigen, am Strassenverkehr teilzunehmen oder Maschinen zu bedienen. Wenn sich nach der Applikation der Augentropfen verschwommenes Sehen einstellt, dürfen Patienten nicht am Strassenverkehr teilnehmen oder Maschinen bedienen, bis diese Beeinträchtigung abgeklungen ist.
Unerwünschte Wirkungen
Die nachfolgenden Nebenwirkungen wurden in klinischen Studien mit Spersadex mono 0,1% berichtet und sind wie folgt unterteilt: «sehr häufig» (≥1/10), «häufig» (<1/10, ≥1/100), «gelegentlich» (<1/100, ≥1/1000), «selten» (<1/1000, ≥1/10000), «sehr selten» (<1/10000) oder «unbekannt» (kann mit Hilfe verfügbarer Daten nicht bestimmt werden).
Erkrankungen des Nervensystems:
Gelegentlich: Dysgeusie.
Augenerkrankungen:
Häufig: Okulärer Diskomfort.
Gelegentlich: Keratitis, Konjunktivitis, trockenes Auge, durch Vitalfärbung der Hornhaut sichtbare Defekte, Photophobie, Verschwommene Sicht, Juckreiz, Fremdkörpergefühl, verstärkter Tränenfluss, anormale Sinnesempfindungen im Auge, Lidrandverkrustungen, Irritationen, okuläre Hyperämie.
Zusätzliche unerwünschte Wirkungen nach Markteinführung:
Erkrankungen des Immunsystems:
Unbekannt: Hypersensitivität.
Endokrine Erkrankungen:
Unbekannt: Cushing-Syndrom, Nebenniereninsuffizienz.
Erkrankungen des Nervensystems:
Unbekannt: Schwindel, Kopfschmerzen.
Augenerkrankungen:
Unbekannt: Glaukom, ulzerative Keratitis, erhöhter Intraokulardruck, verminderte Sehschärfe, Erosion der Kornea, Ptosis, Augenschmerzen, Mydriasis.
Nebenwirkungen, die im Zusammenhang mit phosphathaltigen Augentropfen gemeldet wurden
Sehr selten wurden Fälle von Hornhautkalzifizierungen unter der Therapie mit phosphathaltigen Augentropfen bei Patienten mit ausgeprägten Hornhautdefekten berichtet.
Überdosierung
Eine Überdosierung durch die korrekte ophthalmische Behandlung ist nicht zu erwarten. Durch die versehentliche orale Einnahme von Spersadex mono 0,1% entstehen üblicherweise keine gravierenden Folgen. Es sollen resorptionsvermindernde Massnahmen getroffen werden.
Eigenschaften/Wirkungen
ATC-Code: S01BA01
Dexamethason (Dexamethasonum) gehört zu den für den ophthalmologischen Anwendungsbereich am stärksten wirksamen Kortikosteroiden.
Studien am Tier sowie am Menschen haben gezeigt, dass Dexamethason nach oraler Verabreichung ca. 6× so potent wie Prednisolon und mindestens 30× so potent wie Kortison wirkt.
Wirkungsmechanismus
Wie alle entzündungshemmenden Glukokortikoide bewirkt Dexamethason unter anderem eine Hemmung der Phospholipase A2, des ersten Schrittes in der Prostaglandinsynthese.
Im Weiteren hemmt Dexamethason die chemotaktische Einwanderung von neutrophilen Zellen in den Entzündungsherd.
Pharmakokinetik
Am Kaninchenauge wurden nach einmaliger Applikation von 50 µl einer 0,1% 14C markierten Dexamethasonphosphatlösung Maximalkonzentrationen von 15 µg/g in der Kornea resp. 1 µg/g im Kammerwasser gemessen.
Über das Ausmass einer möglichen systemischen Resorption von Dexamethason nach lokaler Anwendung am Auge liegen keine Angaben vor.
Präklinische Daten
Mutagenes und tumorerzeugendes Potential
Dexamethason ist unzureichend auf mutagene Wirkungen untersucht.
Bei der empfohlenen klinischen Dosis zeigen konventionelle präklinische Studien zur Toxizität bei wiederholter Verabreichung, zur Genotoxizität, zur Karzinogenität oder zur Reproduktion und Entwicklung keine besonderen Gefahren für den Menschen.
Reproduktionstoxizität
Dexamethsaon ruft im Tierexperiment bei Mäusen, Ratten, Hamstern, Kaninchen und Hunden Gaumenspalten und in geringem Umfang andere Fehlbildungen hervor. Beim Menschen liegen aus bisher publizierten Fällen keine Hinweise auf ein erhöhtes Missbildungsrisiko vor. Die Fallzahlen sind jedoch zu gering, um ein Risiko mit Sicherheit ausschliessen zu können.
Sonstige Hinweise
Haltbarkeit
Spersadex mono 0,1% Augentropfen bei Raumtemperatur (15-25 °C) aufbewahren. Flasche nach Gebrauch sofort verschliessen. Nach Anbruch nicht länger als einen Monat verwenden.
Spersadex mono 0,1% Augentropfen sind in ungeöffneter Packung nur bis zu dem auf der Packung mit «EXP» bezeichneten Datum verwendbar.
Hinweise für die Handhabung
Die Tropfenspitze darf weder mit den Händen noch mit dem Auge in Berührung kommen.
Zulassungsnummer
31069 (Swissmedic).
Zulassungsinhaberin
OmniVision AG, 8212 Neuhausen.
Stand der Information
Oktober 2018.
Composition
Principe actif: Dexamethasoni natrii phosphas.
Excipients: Conserv.: Benzalkonii chloridum, Excipiens ad solutionem.
Forme galénique et quantité de principe actif par unité
Collyre: Dexamethasoni natrii phosphas 1 mg/ml.
Indications/Possibilités d’emploi
Conjonctivites de nature non infectieuse, kératites et blépharites en particulier d'origine allergique, inflammations de l'uvée antérieure (iritis, iridocyclite), sclérite, épisclérite et myosite orbitaire. Ophtalmie sympathique.
Posologie/Mode d’emploi
Adultes, adolescents et enfants à partir de 2 ans
Instiller 3 à 5×/jour 1 goutte dans le sac conjonctival.
Cas aigus: jusqu'à 1 goutte toutes les heures. Si aucune amélioration n'est intervenue après 7 à 8 jours de traitement, d'autres mesures thérapeutiques sont à envisager.
Enfants âgés moins de 2 ans
En raison du risque de réactions aux glucocorticoïdes systémiques, l'utilisation chez les enfants de moins de 2 ans n'est pas recommandée.
Contre-indications
- Hypersensibilité au principe actif ou à un des adjuvants.
- Traumatismes et ulcérations de la cornée.
- Herpes simplex (keratitis dendritica), vaccine, varicelle et toutes les autres affections virales de la cornée et de la conjonctive.
- Infections oculaires à mycobactéries.
- Mycose oculaire ou parasitose oculaire non traitée.
- Infections bactériennes de l'œil.
- Glaucome.
- L'utilisation d'un stéroïde est généralement déconseillée après l'élimination facile d'un corps étranger de la cornée.
- Il est en outre déconseillé d'administrer Spersadex mono 0,1% aux nouveau-nés.
Mises en garde et précautions
Précautions générales
Les corticostéroïdes peuvent causer une résistance aux infections bactériennes, virales, fongiques ou parasitaires et favoriser leur installation, tout en masquant les signes cliniques de l'infection.
Une infection fongique doit être envisagée en cas d'ulcération de la cornée. En présence d'une infection fongique, arrêter le traitement par corticostéroïdes.
L'application de Spersadex mono 0,1% pendant une période de temps prolongée peut conduire à un retard de cicatrisation. Un traitement concomitant par anti-inflammatoires non stéroïdiens (AINS) ou un traitement systémique par corticostéroïdes retardent également la cicatrisation (voir «Interactions»).
En cas de maladies entraînant un amincissement de la cornée ou de la sclère, l'utilisation de stéroïdes peut entraîner des perforations.
De même, il peut conduire à une augmentation de la pression intraoculaire et par conséquent à un glaucome, des lésions du nerf optique, une baisse de l'acuité visuelle et un affaiblissement de la vue. Le patient doit être examiné régulièrement pendant le traitement par Spersadex mono 0,1%; avec des contrôles réguliers de la tension intraoculaire. Ce suivi est particulièrement important chez les enfants et les adolescents, car une hypertension oculaire induite par les corticostéroïdes peut survenir plus rapidement que chez les adultes.
Après un usage intensif ou prolongé en continu, la résorption systémique de la dexaméthasone administrée par voie oculaire peut provoquer l'apparition d'un syndrome de Cushing et/ou d'une suppression surrénalienne chez les patients prédisposés, y compris les enfants et les patients traités par le ritonavir (voir «Interactions»). Dans un tel cas, le traitement ne doit pas être interrompu brutalement, mais en réduisant progressivement les doses.
Et d'autres effets systémiques des glucocorticoïdes ne peuvent pas être exclus en cas de traitement prolongé à fortes doses.
La perméabilité élevée de la lentille peut entraîner une cataracte postérieure subcapsulaire. Le risque de cataracte est accru chez les patients ayant une prédisposition, par ex. les diabétiques, particulièrement ceux de type I.
Spersadex mono 0,1% ne doit être prescrit qu'après un examen minutieux de l'œil du patient.
Porteurs de lentilles de contact
Il est déconseillé de porter des lentilles de contact pendant le traitement d'une inflammation oculaire. Spersadex mono 0,1% contient du chlorure de benzalkonium, qui peut causer des irritations oculaires et dont on sait qu'il décolore les lentilles de contact souples. Evitez le contact avec des lentilles de contact souples. Si le médecin juge que le port de lentilles de contact est possible, il doit donner instruction au patient d'enlever les lentilles de contact avant l'administration de Spersadex mono 0,1% et d'attendre au moins 15 minutes avant de les remettre.
Enfants et adolescents
En raison du risque de réactions systémiques, l'utilisation chez les enfants de moins de 2 ans n'est pas recommandée.
Interactions
L'utilisation concomitante de Spersadex mono 0,1% et d'un mydriatique élève le risque d'une augmentation de la pression intraoculaire.
L'association de Spersadex mono 0,1% et d'un médicament contre le glaucome peut affecter les effets des produits appliqués.
L'utilisation concomitante de corticostéroïdes topiques et d'AINS topiques peut accroître le risque de problèmes de cicatrisation de la cornée (voir «Mises en garde et précautions»).
Chez les patients traités par ritonavir, les concentrations plasmatiques de dexaméthasone peuvent, le cas échéant, être augmentées (voir «Mises en garde et précautions»).
Grossesse/Allaitement
Grossesse
Il n'existe pas d'études adéquates ou bien contrôlées concernant l'évaluation de Spersadex mono 0,1% chez la femme enceinte. L'utilisation prolongée ou répétée de corticostéroïdes a été associée à un risque accru de retard de croissance intra-utérin. Les enfants nés de mères ayant reçu des doses importantes de corticostéroïdes pendant la grossesse doivent être surveillés attentivement afin de repérer les signes d'une insuffisance surrénalienne (voir «Mises en garde et précautions»). Des études sur l'animal ont mis en évidence une toxicité pour la reproduction après administration systémique. En outre, l'administration par voie oculaire de dexaméthasone à 0,1% a provoqué des anomalies fœtales chez le lapin (voir «Données précliniques»).
L'utilisation de Spersadex mono 0,1% pendant la grossesse est déconseillée.
Allaitement
On ne sait pas si Spersadex mono 0,1% passe dans le lait maternel humain. Il n'existe aucune donnée concernant le passage de la dexaméthasone dans le lait maternel humain. Il est peu probable qu'à la suite de l'utilisation du produit par la mère, le lait maternel présente une quantité de dexaméthasone décelable ou susceptible d'avoir des répercussions cliniques sur l'enfant.
Il n'est pas possible d'exclure l'existence d'un risque pour l'enfant allaité. Il importe de peser les avantages de l'allaitement pour l'enfant et l'intérêt du traitement pour la mère afin de décider s'il y a lieu d'interrompre l'allaitement ou de renoncer au traitement.
Effet sur l’aptitude à la conduite et l’utilisation de machines
Une vue floue transitoire et d'autres troubles visuels peuvent diminuer l'aptitude à participer au trafic routier ou à utiliser des machines. Si la vue devient floue après l'application du médicament, les patients devront attendre la disparition de la gêne avant de participer au trafic routier ou d'utiliser des machines.
Effets indésirables
Les effets indésirables suivants ont été rapportés dans des études cliniques menées avec Spersadex mono 0,1% et sont classés de la manière suivante: «très fréquents» (≥1/10), «fréquents» (<1/10, ≥1/100), «occasionnels» (<1/100, ≥1/1000), «rares» (<1/1000, ≥1/10'000), «très rares» (<1/10'000) ou fréquence indéterminée (ne peuvent être estimés sur la base des données disponibles).
Affections du système nerveux:
Occasionnels: dysgueusie.
Affections oculaires:
Fréquents: inconfort oculaire.
Occasionnels: kératite, conjonctivite, sécheresse oculaire, défauts visibles liés à la coloration vitale de la cornée, photophobie, vision trouble, prurit, sensation de corps étranger, larmoiement accru, sensations anormales dans l'œil, formation de croûtes sur le bord de la paupière, irritations, hyperémie oculaire.
Effets indésirables supplémentaires après commercialisation:
Affections du système immunitaire:
Fréquence indéterminée: hypersensibilité.
Affections endocriniennes:
Fréquence indéterminée: syndrome de Cushing, insuffisance surrénalienne.
Affections du système nerveux:
Fréquence indéterminée: vertiges, céphalées.
Affections oculaires:
Fréquence indéterminée: glaucome, kératite ulcéreuse, augmentation de la pression intraoculaire, acuité visuelle diminuée, érosion cornéenne, ptosis, douleurs oculaires, mydriase.
Effets indésirables rapportés en lien avec l'utilisation de collyres contenant des phosphates
Très rarement, des cas de calcifications de la cornée sous traitement par des collyres contenant des phosphates ont été rapportés chez des patients présentant des défauts cornéens prononcés.
Surdosage
Lors d'une administration correcte, il est improbable qu'un surdosage se produise.
L'application accidentelle par voie orale de Spersadex mono 0,1% n'entraîne normalement aucune conséquence grave. Il convient de prendre des mesures visant à limiter la résorption du principe actif.
Propriétés/Effets
Code ATC: S01BA01
La dexaméthasone (Dexamethasonum) compte au nombre des corticostéroïdes les plus efficaces utilisés en ophtalmologie.
Les études chez l'animal et l'homme ont montré que la dexaméthasone, après application orale, agit env. 6× plus efficacement que la prednisolone et au moins 30× plus efficacement que la cortisone.
Mécanisme d'action
Comme tous les glucocorticoïdes anti-inflammatoires, la dexaméthasone provoque une inhibition sélective de la phospholipase A2, c'est-à-dire de la première phase de la biosynthèse des prostaglandines.
Elle inhibe en outre la migration chimiotactique des neutrophiles vers le foyer inflammatoire.
Pharmacocinétique
Des concentrations maximales de 15 µg/g dans la cornée et de 1 µg/g dans l'humeur aqueuse de l'œil du lapin ont été atteintes après une seule application de 50 µl d'une solution à 0,1% de phosphate de dexaméthasone marquée au 14C.
On ne dispose d'aucune indication quant à l'importance d'une éventuelle résorption systémique lors de l'application locale de dexaméthasone.
Données précliniques
Potentiel mutagène et tumorigène
La dexaméthasone n'a pas fait l'objet d'études suffisantes sur les effets mutagènes.
A la dose clinique recommandée, des études précliniques conventionnelles de la toxicité après administration répétée, de la génotoxicité, du potentiel carcinogène ou de la toxicité pour la reproduction et le développement ne font apparaître aucun risque particulier pour l'homme.
Toxicité de reproduction
Dans des expérimentations animales chez la souris, le rat, le hamster, le lapin et le chien, la dexaméthasone provoque des fentes palatines et, dans une faible mesure, d'autres malformations. Chez l'être humain, les cas publiés jusqu'ici n'indiquent aucun argument en faveur d'un risque accru de malformations. Le nombre de cas est cependant trop faible pour pouvoir exclure avec certitude un risque.
Remarques particulières
Stabilité
Spersadex mono 0,1% collyre doit être conservé à une température ambiante (15–25 °C). Refermer le flacon immédiatement après l'emploi. Ne pas l'utiliser plus de 1 mois après l'avoir entamé. En emballage non ouvert, le collyre Spersadex mono 0,1% est utilisable jusqu'à la date imprimée sur l'emballage avec la mention «EXP».
Remarques concernant la manipulation
Il faut éviter un contact de l'œil ou de la main avec la pointe du flacon.
Numéro d’autorisation
31069 (Swissmedic).
Titulaire de l’autorisation
OmniVision AG, 8212 Neuhausen.
Mise à jour de l’information
Octobre 2018.
Відгуки (0)
Рекомендовані товари
Ви переглядали

Безкоштовна консультація досвідченого спеціаліста
Опишіть симптоми або потрібний продукт - ми допоможемо підібрати його дозування або аналог, оформити замовлення з доставкою додому або просто проконсультуємо.
Нас 14 спеціалістів і 0 ботів. Ми завжди будемо з вами на зв'язку і зможемо зв'язатися в будь-який час.







 Deutsch
Deutsch French
French Italian
Italian

![Acular Gtt Opht Fl 5 мл [!] Acular Gtt Opht Fl 5 мл [!]](https://apteka-zurich.com/image/cache/catalog/2020-06/PICBACK3D/500_91224-320x320.jpg)
![Acular Gtt Opht Fl 5 мл [!] Acular Gtt Opht Fl 5 мл [!]](https://apteka-zurich.com/image/cache/catalog/2020-06/PICFRONT3D/500_91128-200x200.jpg)